专注于治疗囊性纤维化(CF)患者的制药公司Nivalis近日公布了公司2期试验的初期结果。
试验设计为在携带两份F508del-CFTR突变、一直接受Orkambi™治疗的成年CF患者中评估两个不同剂量(200mg和400mg)Cavosonstat用药的有效性和安全性。结果显示,Cavosonstat没有随着计量变化产生毒性,患者对不同剂量的用药耐受性均为良好。
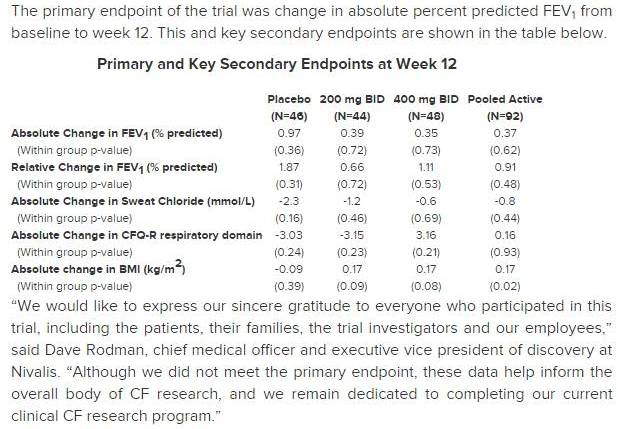
然而,试验未能证明12周治疗后在试验主要终点FEV1预测百分比绝对改变方面、或在汗液氯化物减少方面的益处。
“虽然对试验结果感到失望,但我们计划继续研究cavosonstat和S-亚硝基谷胱甘肽还原酶(GSNOR)抑制剂组合的潜力,好做下一步打算,”Nivalis公司董事长兼首席执行官Jon Congletion说。
关键数据概要
该试验预期的主要终点是FEV1预测百分比从基线到12周的绝对改变。
实验失败后,Nivalis公司首席医疗官兼执行副总裁Dave Rodman宣布:“尽管我们没有达到主要终点,但这些数据帮助认识到CF研究的整体框架,同时我们会继续致力于完成现有的临床CF研究项目。”
数据来源是一项2期、双盲、随机、安慰剂对照、平行组试验。这项试验在携带两个拷贝F508del-CFTR突变并一直接受Orkambi治疗的成年CF患者中评估两个剂量Cavosonstat每日两次给药的有效性和安全性。
该试验共计包括138名成人,分别接受cavosonstat(200mg)与Orkambi治疗(n=44);cavosonstat(400mg)与Orkambi治疗(n=48);安慰剂与Orkambi治疗(n=46);为期16周。试验还包含4周的撤药与随访期,安排在患者完成12周的治疗之后。
关于囊性纤维化
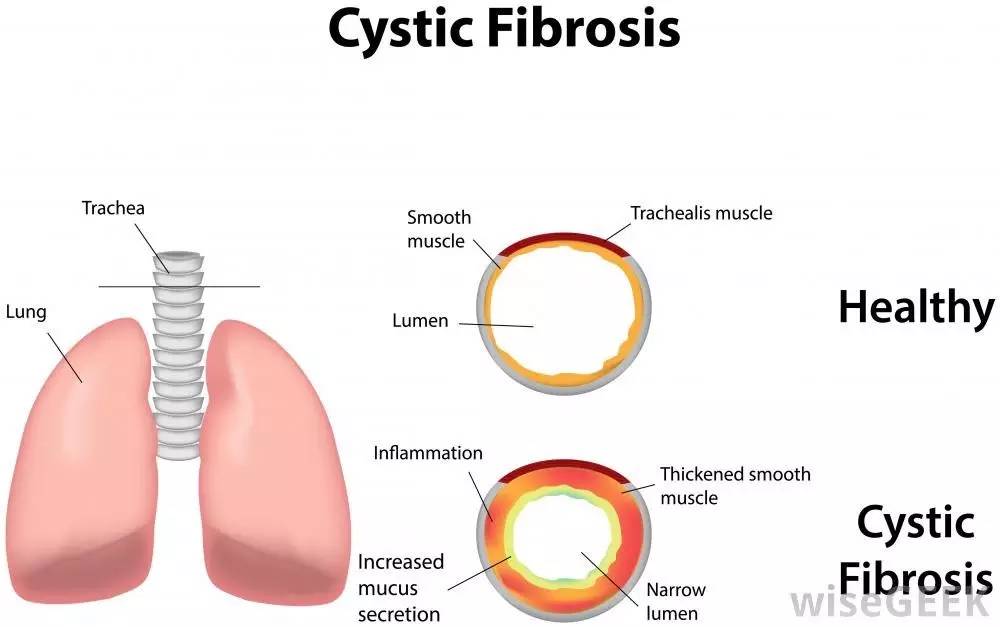
囊性纤维化(CF)是一种致命的遗传性罕见病。患病群体主要分布在美国和欧洲。囊肿性纤维化症的症状可以因为患者的年龄、体内器官受影响的程度、以前的治疗以及被其他不同病症感染而有差异。
总而言之,囊肿性纤维化有全身性的影响,其中包括成长方面、呼吸方面、消化系统方面、以及性器官方面。带有囊肿性纤维化症的新生儿会有缓慢的成长率以及肠阻塞的问题,随着患者的成长,其他症状随之出现,其中包括长期性的发育不良、频繁的肺部感染、消化吸收的困难、以及导致不孕症。
关于NivalisTherapeutics公司

NivalisTherapeutics是一家致力于为CF患者发现、开发和商业化疗法的临床阶段制药公司。除了开发能够延长CF患者生命并改善其生活质量的创新性解决方案,Nivalis还计划利用其专利S-亚硝基谷胱甘肽还原酶(GSNOR)抑制剂组合来为其他疾病开发疗法。
原文链接:
--------------------
校审/曹文东、夏蓓
本文由中国罕见病网编译,转载请注明出处。