3年前
投资1.2亿美元收购
如今不得不放弃
困难重重
市场变化
罕见病新药研发之难
可见一斑
这个新药就是治疗脊髓性肌萎缩的olesoxime。
瑞士药企罗氏(Roche)正式宣布,终止olesoxime治疗SMA2型的临床试验。
这个新药是罗氏在2015年花费巨资从Trophos公司购得,但是,三年后就不得不放弃,令人扼腕。
“我们在为脊髓性肌萎缩( SMA) 的患者开发这个分子药方面遇到了很多困难,“罗氏公司在一封致英国SMA患者组织,Treat SMA的一封信中表示。
“ 这些困难集中在: 处方 (olesoxime 的实际液体准备), 最适当的剂量和监管部门 (美国FDA 和欧盟EMA) 要求进行一个新的三期临床研究。”
过去三年中,罗氏一直在寻找合适的开发途径。
2016年, 罗氏开始了OLEOS 研究, 这个18个月的延伸研究, 主要评估 olesoxime 的长期安全和有效性。
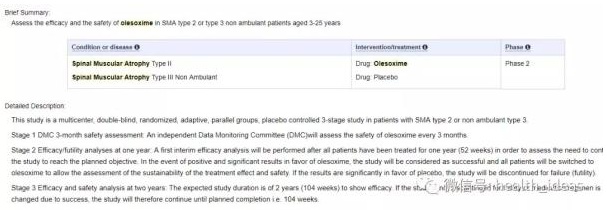
(Olesoxime治疗SMA2临床试验)
今年4月,这个临床试验结果公布,显示,虽然用药后患者症状有所改善,但是,olesoxime的疗效随着时间而消失,到18个月时,疗效已经不在。
与2015年相比,SMA的治疗市场风云变幻。
尤其在2016年圣诞节,这天,美国食品药品监督管理局FDA批准了第一个治疗新药,百健和Ionis公司的Spinraza。
与此同时,新兴的基因治疗方兴未艾。AveXis公司的主打产品AVXS-101, 利用腺相关病毒载体(AAV)技术,将SMN1基因直接运送到体内,期望能根本治疗脊髓性肌萎缩。
SMA是一种严重的神经肌肉疾病,症状是运动神经元的丧失,导致进行性肌无力和瘫痪。
SMA由SMN1基因的遗传缺陷引起,而SMN1是编码运动神经元SMN存活所必需的蛋白质。
SMA的发病率约为10,000例新生婴儿中的一个。
在各个类型的SMA中,最严重形式是1型SMA。1型SMA由于运动神经元丧失和相关肌肉退化,大部分患者在两岁前就需要永久性呼吸支持。
AveXis公司目前进行SVXS-101的三期临床试验,治疗SMA1型患者。
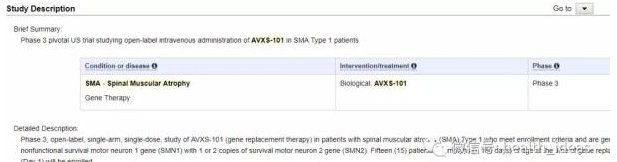
(AVXS-101治疗SMA1型患者的临床试验)
4月,另一家瑞士药企诺华一鸣惊人,以87亿美元的价格收购了AveXis公司。诺华的入局,更加加剧了SMA治疗领域的争夺。
“过去的几年中, SMA 的治疗方案也发生了巨大的变化。 有效治疗的出现, 为新疗法的有效性带来了障碍, 这对我们如何设计和运行我们的临床研究产生了影响。”罗氏无奈表示。
竞争加剧,导致像罗氏一样的大公司也感到压力山大。
所幸的是,这个瑞士药企还有一款治疗SMA的新药,口服的SMN2基因剪接修饰剂,RG7916.
这是罗氏和PTC疗法公司合作的项目,正在进行二期临床试验。
与其继续投资一个疗效不显著,竞争中优势不大的olesoxime,不如集中于RG7916, 罗氏公司的罕见病和患者事务负责人,Sangeeta Jethwa表示。
与此同时,罗氏公司在国内也在积极开展RG7916的临床试验。
SMA治疗新药一览

“我们仍然坚定地承诺SMA 社区, 通过我们的口服 SMN2 剪接修饰剂,RG7916 开发,,这是与 PTC公司 的项目。RG7916 正在进行FIREFISH(火鱼) 和 JEWELFISH(珠珠鱼)的 临床研究。”
“最重要的是, 我们要感谢参与 olesoxime 临床研究的家庭和整个 SMA 患者社区的巨大贡献, 他们每天都激励着我们。”