8月9日,泰格医药申报的维托拉生注射液(viltolarsen)被CDE拟纳入优先审评,用于治疗肌营养蛋白的基因缺失,经验明可通过53号外显子跳跃治疗的杜氏肌营养不良(DMD)。


DMD是一种X连锁隐性遗传病,以神经肌肉退行性病变为特征,通常由抗肌萎缩蛋白(Dys)基因突变引起。儿童发病率较高,每3500~5000名存活男婴中就有1人罹患此病,其肌营养不良蛋白通常不足正常值的3%。全球约有14万例DMD男孩,美国和欧洲约有3万例。患者一般在3~5岁开始发病,最早表现出进行性腿部肌无力(爬楼梯困难),不便行走;12岁时失去行走能力,常年与轮椅为伴;20岁-30岁因呼吸衰竭而死亡。
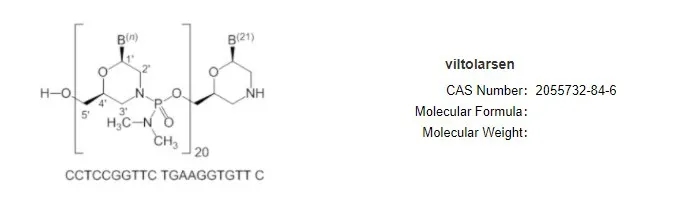
维托拉生是由日本新药株式会社(Nippon Shinyaku)研发的磷酰二胺吗啉代寡聚核苷酸药物。它靶向抗肌萎缩蛋白mRNA前体的剪接过程,通过跳跃抗肌萎缩蛋白(Dys)基因中的外显子53来促进功能性抗肌萎缩蛋白的产生。
在一项II期临床试验(NCT02740972)中,16 名受试者分别随机接受本品或安慰剂治疗4周,然后再接受2个不同剂量(40mg/kg、80mg/kg)的维托拉生开放性治疗20周。结果显示,维托拉生的治疗与平均抗肌萎缩蛋白表达显著增加有关,40mg/kg组和80mg/kg组在试验前的抗萎缩蛋白平均基线水平为0.3%和0.6%,试验后抗肌萎缩蛋白的平均水平分别为5.7%和5.9%。
2020年3月25日,维托拉生在日本获批上市;2020年8月12日,在美国获批上市,此前FDA已授予其罕见儿科疾病认定、孤儿药资格、以及快速通道资格。
希望维托拉生可以尽早在中国上市,造福更多DMD患者。
版权声明:本网站所有注明“来源:罕见病信息网”的文字、图片和音视频资料,版权均属于罕见病信息网网站所有。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。