急性白血病的转化状态需要一定的基因调节程序,而这些程序主要涉及转录因子和染色质调节子。近日,一篇发表在国际杂志Molecular Cell上题为“ZMYND8-regulated IRF8 transcription axis is an acute myeloid leukemia dependency”的研究报告中,来自宾夕法尼亚大学等机构的科学家们通过研究发现,利用CRISPR筛选工具或能识别出一种治疗性靶点来治疗急性髓性白血病(AML),相比当前疗法而言,这或许有望给患者带来更少的副作用,这种名为ZMYND8的靶点或许并不是一种突变基因,而是一种表观遗传调节蛋白,癌细胞需要其来控制对癌细胞存活和生长非常关键的基因表达。

图片来源:https://www.sciencedirect.com/science/article/abs/pii/S1097276521005876?via%3Dihub
研究者Junwei Shi说道,如今我们已经发现,AML患者机体的癌细胞严重依赖于ZMYND8,而且多亏这种复杂的基于CRISPR的筛选方法,我们才能够确定具体的可作为药用的靶点。本文研究结果表明,提供抵御ZMYND8的药物抑制剂或能破坏AML易感基因调节回路,这或许是一个开发比当前治疗方法更好的精准医学化合物的机会,从而就能治疗血液癌症,而这恰恰是研究人员目前正在研究的领域。
AML每年影响着2万多名患者的健康,包括儿童和成年人,而且20岁以上患者的5年生存率仅为27%,标准的治疗手段包括化疗,然而,并非所有患者都会产生反应,因此研究人员需要开发一些新方法来扩大患者的治疗选择并改善其生存率。CRISPR技术不仅能帮助科学家们以比以前手段更加容易且低成本地修饰基因,而且还能帮助他们同时筛选出数千个具有较高治疗靶向潜力的特定功能蛋白结构域。
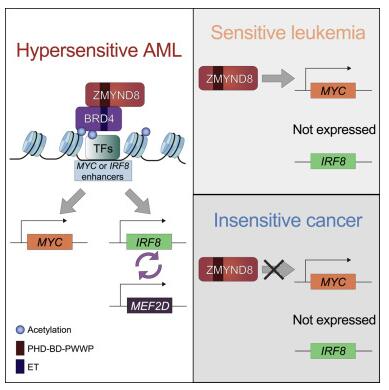
利用CRISPR筛选技术或有望识别出治疗急性髓性白血病的新型药物靶点。
图片来源:Zhendong Cao,et al. Molecular Cell (2021). DOI:10.1016/j.molcel.2021.07.018
文章中,研究人员利用CRISPR技术精确破坏了癌细胞中蛋白质的结构域功能,同时绘制出了其分子功能图谱,并对其修饰用于小鼠模型的研究,结果发现,抑制小鼠机体中ZMYND8的表观遗传阅读功能或能使得小鼠机体的肿瘤更小且生存率更高。此外,研究人员还发现了一种新型生物标志物,即来自AML细胞的基因IRF8的表达水平或表观遗传学状态,利用该生物标志物,研究人员就能预测癌细胞对ZMYND8抑制剂的敏感性。此外,研究者还利用在宾夕法尼亚大学医学院接受治疗的病人的血液样本验证了IRF8的高表达和IRF8增强子DNA元件的存在,从而就支持了其研究发现。
文章的共同作者Shelley L. Berger说道,如今研究人员在癌症中发现了很多遗传和表观遗传学修饰现象,但很少有能用于操控的靶点;本文研究中,研究人员利用CRISPR技术或许揭示了AML所依赖的一种意想不到的表观遗传学关联的分子回路,而且研究人员能对其进行潜在曹龙;这或许就为开发利用新一代表观遗传抑制剂来对这些患者进行更好的治疗打开了一扇大门。综上,本文研究结果表明,ZMYND8或能作为一种潜在的治疗性靶点来调节AML患者机体中必要的转录程序。
原始出处:
Zhendong Cao,Krista A.Budinich,Hua Huang, et al. ZMYND8-regulated IRF8 transcription axis is an acute myeloid leukemia dependency, Molecular Cell (2021). DOI:10.1016/j.molcel.2021.07.018
版权声明:本网站所有注明“来源:罕见病信息网”的文字、图片和音视频资料,版权均属于罕见病信息网网站所有。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。