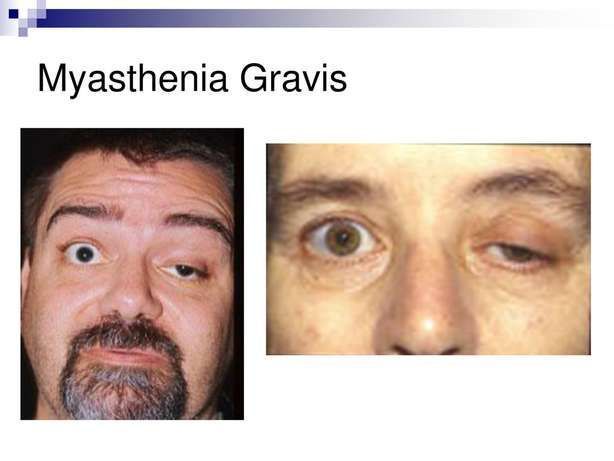
优时比(UCB)近日公布了3期MycarinG研究的阳性顶线结果。该研究正在评估rozanolixizumab与安慰剂治疗全身型重症肌无力(gMG)成人患者的疗效和安全性。rozanolixizumab是一种通过皮下注射(SC)、靶向新生儿Fc受体(FcRn)的单克隆抗体。
结果显示,该研究达到了主要终点:治疗第43天,与安慰剂组相比,rozanolixizumab治疗组患者重症肌无力日常生活活动(MG-ADL)总评分相对基线发生了具有统计学意义和临床意义的变化。此外,该研究的全部次要终点也达到了统计学意义。该研究中,rozanolixizumab的耐受性良好,未发现新的安全信号。
rozanolixizumab是一款在研的FcRn靶向单抗,以高亲和力特异性结合人类FcRn,通过阻断FcRn和IgG的相互作用,来加速IgG的分解代谢,降低致病性IgG自身抗体的水平。目前,rozanolixizumab正被开发通过驱动致病性IgG自身抗体的清除,来治疗多种由致病性IgG自身抗体驱动的自身免疫性疾病,包括gMG、原发性免疫性血小板减少症(ITP)、抗髓鞘少突胶质细胞糖蛋白免疫球蛋白G抗体(MOG-IgG)相关疾病(MOGAD)、自身免疫性脑炎(AIE)。
rozanolixizumab的安全性和有效性尚未确定,并且尚未获全球任何监管机构批准用于任何适应症。MycarinG研究的最终数据和其他细节将在2022年召开的医学会议上公布。
上述研究中令人鼓舞的发现,显示了rozanolixizumab在治疗gMG方面的潜力,并进一步强化了抑制FcRn可能是治疗该疾病的一种有希望的方法。根据这些结果,优时比预计从2022年第三季度开始,在美国、欧盟、日本提交rozanolixizumab治疗gMG的上市申请文件。
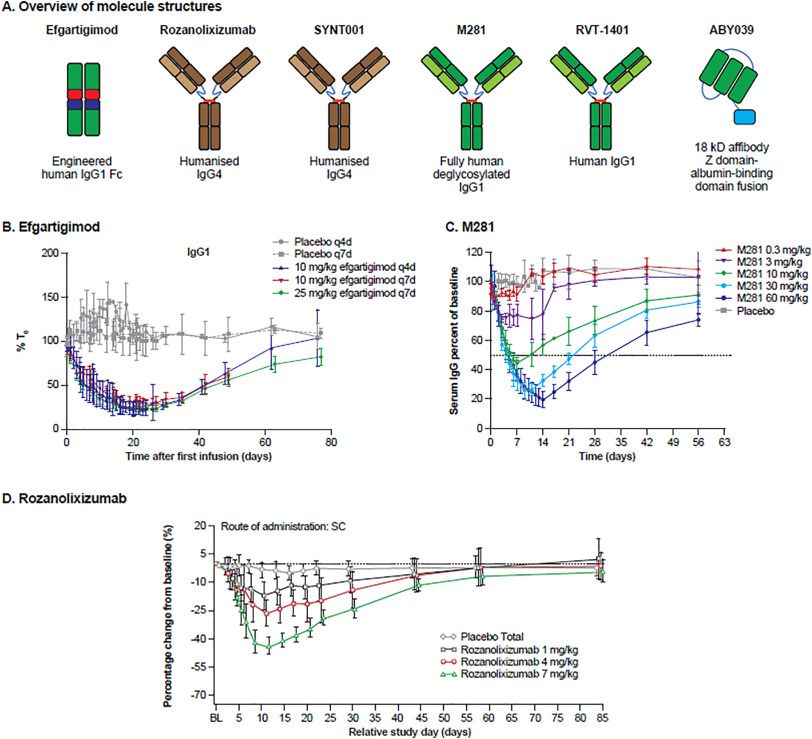
除了rozanolixizumab之外,优时比还正在调查其在研药物zilucoplan(补体成分5的肽抑制剂,C5抑制剂)是否能为gMG患者提供患者价值。来自RAISE研究的初步结果预计将在未来几周内公布。zilucoplan的安全性和有效性尚未确定,该药也尚未获全球任何监管机构批准用于任何适应症。
重症肌无力(MG)的治疗选择非常有限。鉴于该病可引起广泛的症状,其中一些症状可能需要紧急干预或住院治疗,因此迫切需要新的治疗方案来解决MG患者群体中显著未得到满足的医疗需求。
优时比的上述2种药物,具有不同但潜在互补的作用机制,这有望为优时比提供一个独特的机会,为患者和医疗专业人员提供选择灵活性,为他们提供最适合其个人需求的用药选择。
重症肌无力(MG)是一种由致病性IgG介导、严重影响生活质量的神经肌肉疾病,疾病症状以及当前疗法的副作用都可能对患者的生命造成重大损害。MG会对患者的生活和独立性产生毁灭性的影响,可能会影响吞咽、说话、行走甚至呼吸的能力。此外,每个患者经历MG的过程都不同,这会使疾病管理变得不可预测。
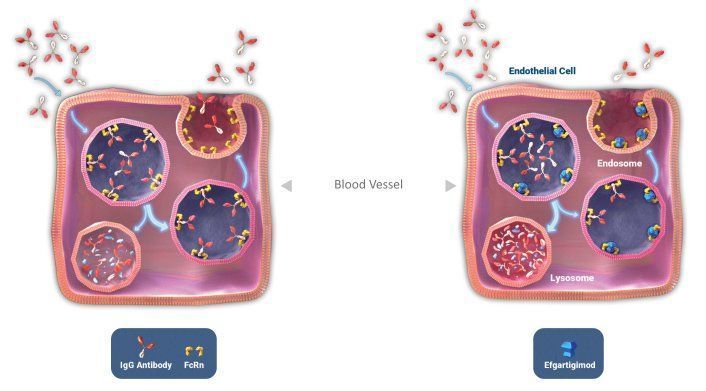
目前,再鼎医药合作伙伴Argenx开发的FcRn拮抗剂efgartigimod治疗gMG的上市申请正在接受美国、日本、欧盟监管机构的审查。美国方面,FDA预计将在2021年12月17日作出审查决定。
如果获批,efgartigimod将成为第一个也是唯一一个获得监管批准的FcRn拮抗剂,将为gMG患者带来一种首创的靶向疗法。来自关键3期ADAPT试验的结果显示,efgartigimod治疗可显著改善gMG患者的力量和生活质量。特别是,大多数接受efgartigimod治疗的患者,在给药的头2周就观察到有临床意义的改善。这些结果对MG社区具有重要意义。
efgartigimod是一款在研的抗体片段,旨在减少致病性IgG抗体并阻断IgG循环。efgartigimod可与FcRn结合,FcRn在全身中都有广泛表达,在阻止IgG抗体的降解过程中起着核心作用。阻断FcRn可降低IgG抗体表达水平,可治疗已知由致病IgG抗体驱动导致的自身免疫性疾病,包括:重症肌无力(MG),一种导致肌肉无力的慢性病;寻常性天疱疮(PV),一种以皮肤严重起泡为特征的慢性皮肤疾病;免疫性血小板减少症(ITP),一种表现为瘀斑和出血的慢性疾病;慢性炎症性脱髓鞘性多发性神经病(CIDP),一种神经系统受损导致运动障碍的疾病。
2021年1月6日,再鼎医药与argenx宣布,双方已达成独家授权合作,再鼎医药将负责推进efgartigimod在大中华区(包括中国内地、香港、台湾和澳门地区)的开发和商业化工作。
原文出处:UCB announces positive Phase 3 results for rozanolixizumab in generalized myasthenia gravis