脊髓性肌萎缩症(spinal muscular atrophy,SMA)为常染色体隐性遗传。其致病基因SMN1位于 5q13.2,编码运动神经元存活蛋白。
根据国内常见报道,SMA发病率为 1/10000,携带率为1/50,90%婴幼儿期发病,50%在2岁前死亡。预计中国SMA现存患者人数大约3-5万人,每年新增1200人。
另根据2017年发表的一份综述文章《Prevalence, incidence and carrier frequency of 5q–linked spinal muscular atrophy – a literature review》,估计全球范围内SMA的患病率为1-2/10万,每一万名活产婴儿中约有1人发病,其中Ⅰ型SMA约占所有病例的60%。
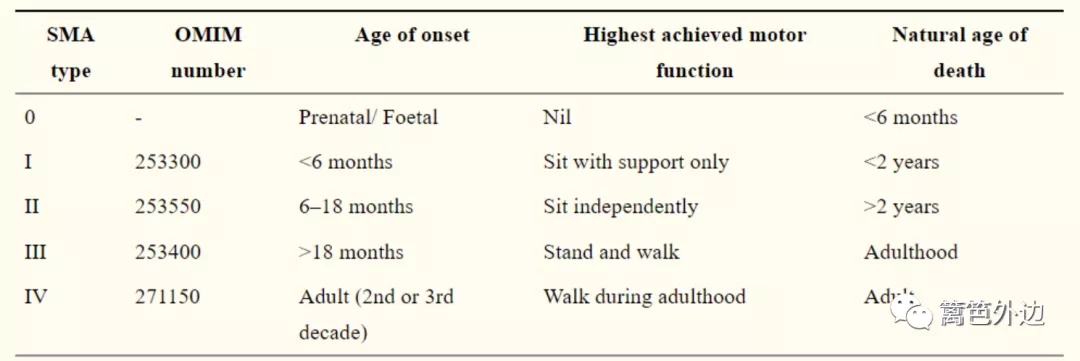
Ⅰ型SMA 发病于6月龄以下婴幼儿,通常2岁以前死亡,占总发病率的60%;
Ⅱ型SMA发病于6-18月龄婴幼儿,通常2岁以后死亡,
Ⅲ型SMA发病于18月龄以上婴幼儿,通常成年后死亡,
Ⅳ型SMA发病于成年时期,通常为20-30岁发病,寿命不受影响;
此外,还有0型SMA,发病于胎儿期,在出生前或出生后6月内死亡。
由于0、Ⅰ型SMA 患者预期寿命极短,因此SMA存活患者多为Ⅱ型和Ⅲ型,患病率约1.5/10万。
此外,根据该综述研究结果显示,SMA在亚洲人和白种人中具有更高的基因携带率,发病率估计约为1/8000,而黑人和西班牙裔人群的发病率估计较低,约为1/20000。
按患病率2/10万粗略估算,SMA全球患者数量约16万人,且以欧美白人和亚洲人群为主。幸运的是,欧美发达国家具备更高的药品支付能力,占亚洲人口1/3的中国也将诺西那生钠纳入了国家医保目录。
如果我们认为欧美发达国家和中日韩等亚洲发达国家具备该产品的购买力,那么,诺西那生钠潜在的购买群体约有7.4万人,其中2.8万患者在中国,占据了诺西那生钠潜在买家的38%。
诺西那生钠自2009年前立项开发,2012年Ionis(原ISIS,2015年为与恐怖组织ISIS区分而改名Ionis)将全球市场权益出售给Biogen,出售费用含2900万美元首付款和4500万美元里程碑付款。同时,根据Biogen2016年的年报数据,诺西那生钠的总许可费用为7500万美元。因此,可以推测,渤建在诺西那生钠的开发费用上应不超2亿美元。

2016年12月,诺西那生钠在美国上市;
2017年6月,在欧盟上市;
2017年8月,在加拿大、巴西等国上市;
2017年9月,日本上市,;
2017年11月,澳大利亚上市;
2018年1月,土耳其上市;
2019年1月,宝岛台湾上市;
2019年4月,在中国大陆上市;
2019年8月,俄罗斯上市.......
至此,诺西那生钠已在全球六个大洲、50多个国家上市。
年报数据显示,诺西那生钠在2016年上市首年仅销售几百万美元,但2017年快速增长至8.84亿美元,2018年达到17亿美元,2019年21亿美元,2020年下滑至20.5亿美元,2021年上半年销售10.2亿美元。
可以预见的是,诺西那生钠的全球市场规模已经到顶。而截止到本轮国家医保谈判前,渤建已靠诺西那生钠实现了77.5亿美元的收入,开发成本也早已收回。
因此,可以猜测,诺西那生钠本轮国谈如此迫切的进入中国国家医保目录,主要有几点因素:
1. 其研发成本早已收回,未来就是赚多赚少的问题;
2. 中国拥有占全球38%的SMA患者尚未接受治疗,通过降价提高可及性,并博取个好名声,不失为双赢选择;
3. 诺西那生钠在中国是豁免临床上市,意味着其在中国的开发费用更低;
4. 第四点则是来自于竞品的压力。
根据诺西那生钠临床研究数据显示,诺西那生钠仅可使患儿死亡或永久通气的风险降低47%,而并不能实现临床治愈。有报道其针对Ⅰ型SMA患儿可增加约5年寿命,质量调整年约3年。
而诺华2019年5月上市的全球第二款SMA治疗药物“Zolgensma”,仅需一针,便可实现Ⅰ型SMA患者的长期缓解甚至治愈!同时,这款基因治疗药物已于2021年10月21日在中国申报临床。
此外,另一款治疗SMA的口服药物“利司扑兰”也已于2021年6月在中国上市,国内定价为6.38万/瓶,患儿年治疗费用为30-100万元,但遗憾的是,其缺席了本轮医保谈判。
显然,不足3万患者的SMA罕见病市场,留给渤建的时间不多了,抢在竞品前占据更多的市场则显得更有意义。
但对于患者而言,仅增加5年预期寿命显然不是最佳的选择,而诺华一针治愈的产品才是上上选。
期待该产品尽早在中国上市,并尽早进入国家医保目录。即便一针10万,中国每年新增的1200名患儿也是极为庞大的市场!!!
写在最后,任何一个群体都不应被忽视。相信在中国这场大跃进式的创新大潮下,越来越多的小群体会获得平等呼吸的权利。