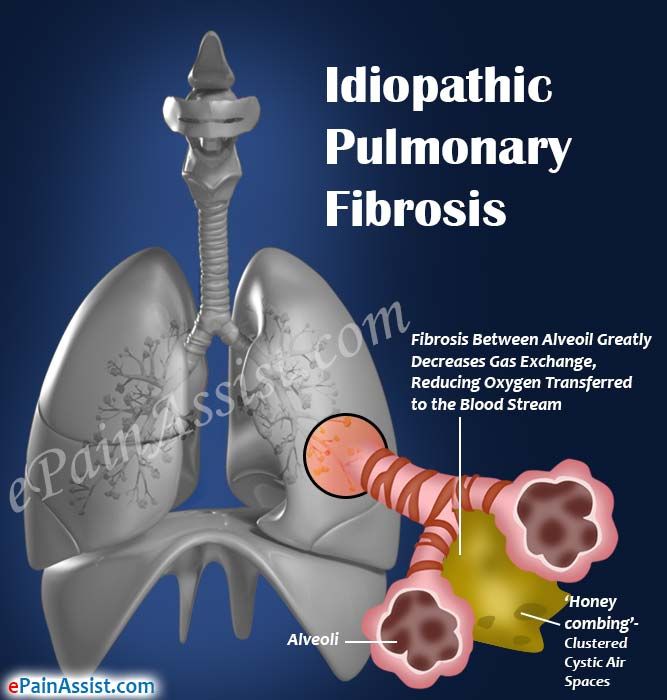
特发性肺纤维化-IPF(图片来源:epainassist.com)
Horizon Therapeutics公司近日宣布,评估HZN-825治疗特发性肺纤维化(IPF)的2b期关键试验对入组了首例患者。HZN-825是一种溶血磷脂酸受体1(LPAR1)拮抗剂,开发用于治疗IPF,这是最常见的间质性肺病(ILD)。临床前研究表明,靶向LPAR1有可能预防并可能逆转IPF的内在病理学特征。
IPF是一种罕见的进行性肺部疾病,由肺部炎症和纤维化或疤痕引起。其特征是呼吸困难、慢性咳嗽和潜在死亡。在美国大约有10万人患有IPF,该疾病的中位生存期不到5年。
该试验中,大约360例患者将以1:1:1的比例接受接受HZN-825 每日一次300mg、每日2次300mg、安慰剂,治疗52周。主要终点是52周后用力肺活量(FVC)的变化。这是一个测量肺活量的客观终点,用于评估肺部疾病的进展和治疗的有效性。次要终点包括6分钟步行试验(6MWT)、King’s-Brief间质性肺病(K-BILD)问卷、因呼吸窘迫住院率,以及无进展生存期的复合终点。患者入组预计需要大约2年时间。
HZN-825是一种口服选择性LPAR1拮抗剂,已显示出对系统性硬化症(SSc)有临床影响的早期迹象。LPAR1信号与纤维化和炎症有关,临床前和临床证据支持LPAR1拮抗剂在多个器官系统(包括肺和皮肤)中的抗纤维化潜力。
在上述2b期关键试验启动之前,对早期弥漫性皮肤系统性硬化症患者进行了2a期试验,获得了令人鼓舞的疗效和安全性数据。2018年完成的HZN-825治疗弥漫性皮肤系统性硬化症的安慰剂对照8周试验显示出积极的反应趋势,改良Rodnan皮肤厚度评分(简称mRSS)表现改善,这是2b期关键试验的次要终点。
此外,2a期试验16周开放标签延长期的数据表明,更长的治疗时间可能会显示出更有意义的益处。在接受24周治疗的患者中,79%的mRSS有临床意义的改善。
原文出处:Horizon Therapeutics plc Announces First Patient Enrolled in Phase 2b Pivotal Trial Evaluating HZN-825 for the Treatment of Idiopathic Pulmonary Fibrosis (IPF)