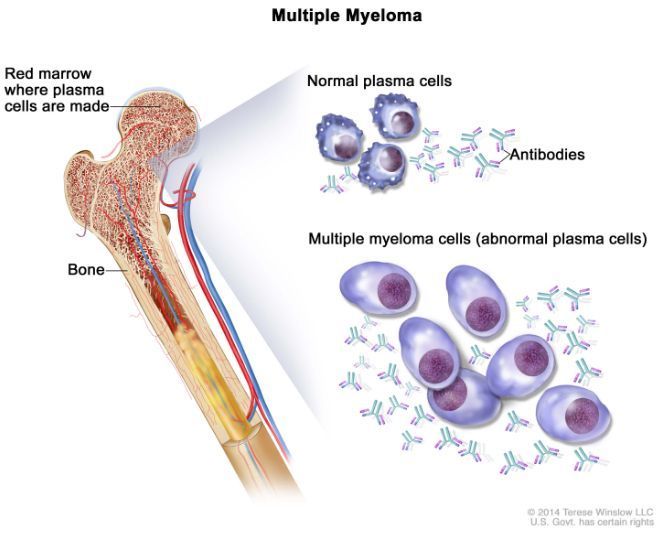
多发性骨髓瘤(图片来自:cancer.gov)
传奇生物(Legend Biotech)与合作伙伴强生(JNJ)旗下杨森制药近日联合宣布,由传奇生物自主研发的嵌合抗原受体T细胞(CAR-T)疗法西达基奥仑赛(英文商品名:Carvykti,通用名:ciltacabtagene autoleucel,简称cilta-cel)已获得欧盟委员会(EC)有条件批准:用于治疗既往接受过至少3种治疗(包括免疫调节剂[IMiD]、蛋白酶体抑制剂[PI]、抗CD38单克隆抗体)、并且在最后一次治疗中被证实疾病进展的复发和难治性多发性骨髓瘤(RRMM)成人患者。
在美国,Carvykti于2022年2月底获得批准,用于治疗既往接受过4种或4种以上治疗(包括PI、IMiD、抗CD38单克隆抗体)的复发或难治性多发性骨髓瘤(R/R MM)成人患者。
值得一提的是,Carvykti是首个国内自主研发在海外获批上市的细胞疗法。Carvykti是一款具有2种靶向B细胞成熟抗原(BCMA)单域抗体的CAR-T细胞疗法,以一次性输液的方式给药。
此次批准基于关键性CARTITUDE-1研究的结果。该研究纳入了的RRMM患者既往接受的治疗方案中位数为6种(范围:3-18种),数据显示,Carvykti一次性治疗实现了早期、深度持久的缓解:在18个月的中位随访时间中,总缓解率(ORR)高达98%(95%CI:92.7-99.7),80%的患者获得了严格的完全缓解(sCR)。sCR是一种医生在治疗后无法通过成像或其他测试观察到任何疾病迹象或症状的指标。
Carvykti是一种靶向B细胞成熟抗原(BCMA)的嵌合抗原受体T细胞(CAR-T)疗法,使用嵌合抗原受体(CAR)的转基因对患者自身的T细胞进行修饰,以识别和消除表达BCMA的细胞。BCMA主要表达于恶性多发性骨髓瘤B细胞、晚期B细胞和浆细胞的表面。Carvykti的CAR蛋白具有2种BCMA靶向单域抗体,对表达BCMA的细胞具有高亲和力,在与BCMA表达细胞结合后,CAR可促进T细胞活化、扩增,继而清除靶细胞。
2017年12月,杨森与传奇生物签订了全球独家许可和合作协议,以开发和商业化cilta-cel。2019年12月,cilta-cel在美国被授予突破性疗法认定(BTD);2020年8月,cilta-cel在中国被纳入“突破性治疗药物”。在美国、欧盟、日本,cilta-cel均被授予了孤儿药资格(ODD)。
多发性骨髓瘤细胞表面的有效生物治疗靶点(图片来源于文献:PMID:30545798)
多发性骨髓瘤(MM)是仅次于非霍奇金淋巴瘤的第二大常见血液学恶性肿瘤。近年来,尽管在化疗、蛋白酶体抑制剂、免疫调节剂沙利度胺衍生物和CD38靶向抗体方面取得了很大的进展,但几乎所有患者最终仍会复发。因此,对新治疗方案存在着迫切需求。MM市场预计2027年将达到290亿美元。
B细胞成熟抗原(BCMA)是一种极其重要的B细胞生物标志物,广泛存在于MM细胞表面,近年来已成为MM和其他血液系统恶性肿瘤的一个非常热门的免疫治疗靶点。目前,针对BCMA开发的免疫疗法超过20种,主要分为3类:嵌合抗原受体T细胞疗法(CAR-T,百时美施贵宝/蓝鸟生物、诺华为代表)、双特异性抗体(BsAb,安进为代表)、抗体药物偶联物(ADC,葛兰素史克为代表)。
2020年8月,葛兰素史克(GSK)BCMA靶向抗体药物偶联物(ADC)Blenrep(belantamab mafodotin,GSK2857916)获得美国和欧盟批准,成为全球获批的第一种BCMA靶向疗法:用于既往已接受过多种疗法(包括免疫调节剂、蛋白酶体抑制剂、抗CD38抗体)的复发或难治性多发性骨髓瘤(R/R MM)患者。
2021年3月,百时美施贵宝(BMS)BCMA靶向CAR-T细胞疗法Abecma(idecabtagene vicleucel,ide-cel)获得美国FDA批准,成为全球获批的第一种BCMA CAR-T细胞疗法:用于治疗既往接受过4种或更多种疗法(包括免疫调节剂、蛋白酶体抑制剂、抗CD38抗体)的R/R MM成人患者。来自关键2期KarMMa研究的数据显示,总缓解率(ORR)为72%、严格完全缓解率(sCR)为28%,中位缓解持续时间(DoR)为11个月,sCR患者的中位DoR为19个月。