威尔逊病(Wilson disease,WD)是一种罕见的遗传病,会导致铜在肝脏、大脑、角膜、肾脏和心肌中病理性沉积。本文介绍两例伴有进行性运动障碍的神经系统WD,检查 Kayser-Fleischer 环(K-F环)阳性,转氨酶正常,血清铜和铜蓝蛋白低和 24h尿铜增加。颅脑成像显示 T2/FLAIR 对称性基底节高信号。由于其罕见性和表现形式多样,这些病例常被忽视和误诊。需要多种检查明确诊断,且越早干预,预后越好。

背景
英国神经学家塞缪尔·威尔逊(Samuel Wilson)1912 年描述一种神经系统疾病,病理是大脑中的豆状核和肝脏中的肝细胞退化,后被称为“肝豆状核变性”,以其同名威尔逊病 (WD) 更为人知。WD 患病率为15-30/100万,是常染色体隐性遗传病,致病基因ATP7B编码一种铜转运P型ATP酶。转运蛋白的缺乏或排泄胆汁铜的减少,导致铜在肝脏、中枢神经系统、角膜、肾脏和心肌中的过度沉积。临床表现儿童主要是肝脏,青少年和年轻人更可能是神经系统。根据表现不同,分为肌张力障碍;共济失调;帕金森症状。
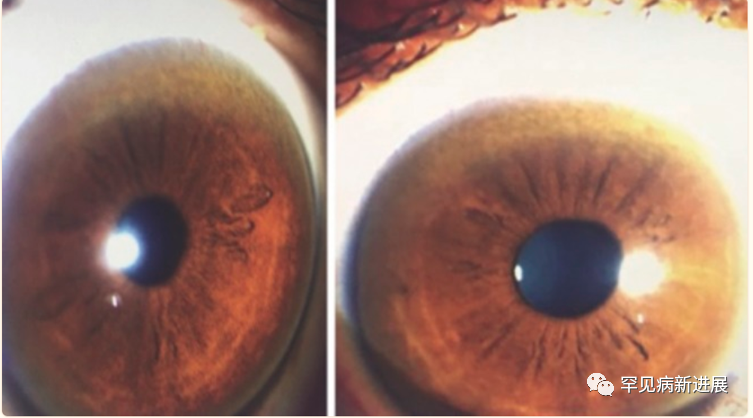
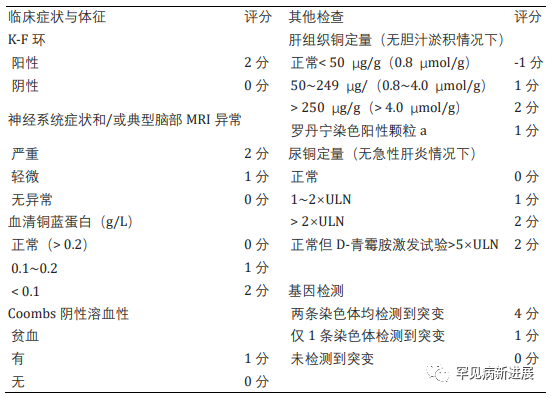
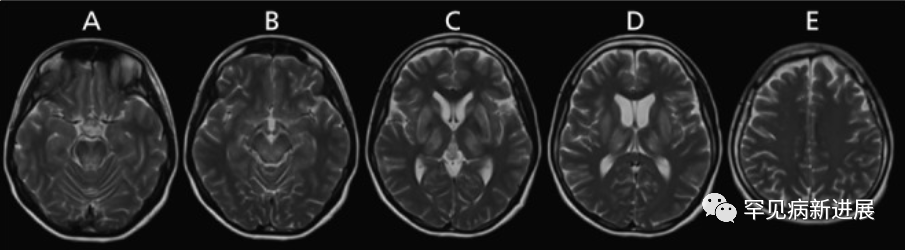
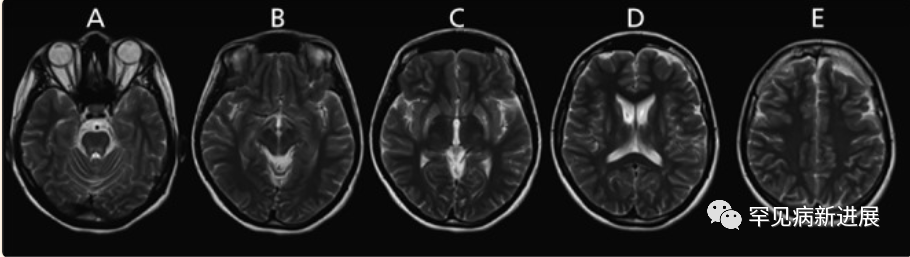
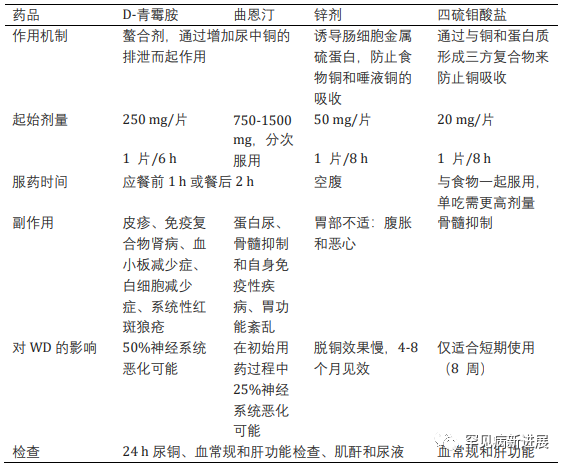
病例情况 病例一:伴有帕金森症状的共济失调型;病例二:伴有帕金森症状的肌张力障碍。两名患者均接受裂隙灯检查有 K-F 环(图1)。 肝脏超声检查有明显结构异常,实验室检查肝功能正常,低血清铜、低铜蓝蛋白和尿铜排泄增加,均无基因检测。(表一) 据统计50% 的肝脏和 99% 的神经系统病变患者有K-F 环(后弹力膜上铜沉积)。 表2: 第8届WD国际会议诊断标准(Leipzig评分) 注:总分≥4分可确诊;总分3分为疑似诊断,需进一步检查;总分≤2分基本不考虑诊断;a:肝铜定量不可及时;ULN:正常值上限 脑部磁共振成像未显示典型的双熊猫征,但在壳核、尾状核和丘脑核上显示对称的 T2/FLAIR 高信号(图 2和图 3)。 两案例均高度暗示了矿物沉积,根据 Leipzig评分,均是 WD 的明确案例。 案例 1 的T2加权序列的代表性图像。背侧区域有高信号B.上中脑轴向切开;中脑被盖上有汇合的高信号C.外侧裂轴向切开;外侧丘脑、尾状核和壳核区有明显的高信号D.岛状区轴向切开;在丘脑和基底神经节可见广泛的双侧高信号E. Corona radiata 轴向切割;双侧半卵圆形未出现任何信号异常 案例 2 的T2加权序列的代表性图像。脑桥背侧区域有高信号B.上中脑轴向切开;黑质C区有外观正常的红色核高信号。壳核上有明显的高信号,有磁化率伪影区域,左侧多于右侧D.侧脑室区域轴向切割,壳核和尾状核上可见连续广泛的高信号E.冠状放射状轴向切割,双侧半卵圆形未见任何信号异常。 由于这种疾病的罕见性,启动基于人群的筛查并不具有成本效益。但对于无法解释的神经系统疾病伴或不伴相关肝病的患者,筛查应该强制性。WD 须与诸如特发性震颤、年轻发病的帕金森病、全身性肌张力障碍和其他罕见的运动障碍(如亨廷顿病、Hallervorden-Spatz 病、特发性扭转性肌张力障碍、舞蹈病-棘红细胞增多症和良性家族性舞蹈病)区分开来。因此,WD 是一种诊断紧急情况,需要立即全面检查。 管理 至于治疗,明确的治疗包括肝移植,特别是对于急性肝炎或暴发性肝功能衰竭的患者。对严重和神经系统后遗症患者,最好的选择是直接增加尿中铜的排泄,即 D-青霉胺和曲恩汀,或阻断胃肠道对铜的吸收,即锌剂和四硫代钼酸盐(表三)。低铜饮食是主要的治疗方法,并补充锌,随后注意到言语、震颤和四肢僵硬的显著改善。第一个病例接受了 D-青霉胺治疗,药物输注缓慢以减少血液不良后果并监测反常的神经功能恶化。至于第二个病例,由于基线神经系统状态相对严重且恶化风险高,该患者继续服用锌补充剂。因无两个相同 WD 患者,治疗应个体化。对螯合剂和药物治疗无效的衰弱性运动障碍患者,可提供肉毒杆菌毒素注射。筛查患者的兄弟姐妹并监测他们的血清铜蓝蛋白也是管理的重要组成部分。早期干预有更好预后,治疗应紧迫。 表三