结节性硬化症(TSC)是一种遗传多系统疾病,涉及脑部、皮肤、肾脏和心脏等方面的症状,而需医学多学科的持续支持。过去几年,TSC领域取得显著进步,包括诊断与疾病管理方法的更新,及mTORC1抑制剂等可用治疗手段更加丰富。本篇综述编译,从基础病理到临床实践,基于多学科疾病管理的视角,总结了TSC各症状类别对应的治疗与随访监测策略。

TSC的病理机制与诊断
TSC的发病机制是由于TSC1或TSC2基因的致病性突变,导致TSC1/TSC2二聚体不再抑制哺乳动物雷帕霉素(mTOR)靶标,mTOR信号通路被过度激活后细胞增殖太快、血管生成。TSC新生儿发病率,估算为1/6000-10000;临床症状为良性非侵袭性肿瘤,又称错构瘤,最常见于脑部、肾脏、心脏和皮肤,不同患者间的症状差异较大。尽管被视为遗传性疾病,70%的TSC患者为散发,属于体细胞突变。精准诊断是TSC患者长期生存和个体化护理的基础。TSC确诊需满足至少两项主要特征,或一项主要特征加两项次要特征。若能检查到TSC1或TSC2基因突变,亦可作为确诊。若发现患者有淋巴管平滑肌瘤病和血管平滑肌脂肪瘤,但无其它症状,则不能确诊,只可计为一项主要特征。
诊断TSC的主要特征:⑴色素脱失斑≥3处,最小直径5 mm;⑵血管纤维瘤≥3处或头部纤维斑块;⑶指/趾甲纤维瘤≥2处;⑷鲨鱼皮肤;⑸多发视网膜错构瘤;⑹脑皮质发育不良≥3处,包括结节和脑白质转移;⑺室管膜下结节;⑻室管膜下巨细胞星形细胞瘤(SEGAs);⑼心脏横纹肌瘤;⑽淋巴肌瘤病;⑾血管平滑肌脂肪瘤≥2处。
诊断TSC的次要特征:⑴皮肤碎纸屑样斑点;⑵牙釉质点凹陷≥3处;⑶口内纤维瘤≥2处;⑷多发性肾囊肿;⑸非肾性错构瘤。
TSC需多学科支持的长期管理
TSC临床症状具异质性,从无特别症状的黑色素减退,到重症的耐药性癫痫、认知缺陷,均可同等几率影响到男、女患者,女性患者往往症状更多。TSC1基因突变型的患者通常症状较轻,而TSC2基因突变型患者较少出现肾、肝、视网膜病变。发生于神经、肾脏的SEGAs及肾血管平滑肌脂肪瘤是最可怕的并发症,导致TSC死亡增加。
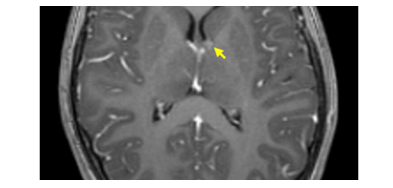
图1 一例儿童TSC患者左脑的SEGA
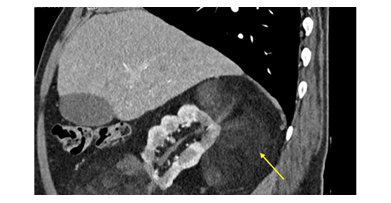
图2 右肾附近的大血管平滑肌脂肪瘤
TSC对器官影响的广泛性和疾病的进展性,需要多学科参与的长期治疗与管理,尚无症状的患者亦不例外(表1)。mTOR通路之于TSC关系的揭露,促进mTORC1抑制剂的开发,很多研究证实其对多种TSC症状有疗效。雷帕霉素(Rapamycin)及其衍生物依维莫司(Everolimus)已投入临床使用。雷帕霉素是一种大环内酯类化合物,和其类似物一样,都可通过与FKBP12结合后抑制TORC1,其证据来自于EXIST-1和2临床研究。mTOR抑制剂治疗的不良反应包括感染、口炎、痤疮、闭经、高胆固醇血症和其他代谢紊乱,停药之后疾病容易反弹,长期用药不良反应尚待关注(表2)。
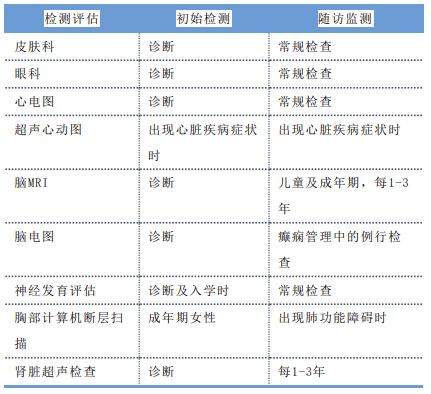
表1 对无症状TSC患者的检测建议
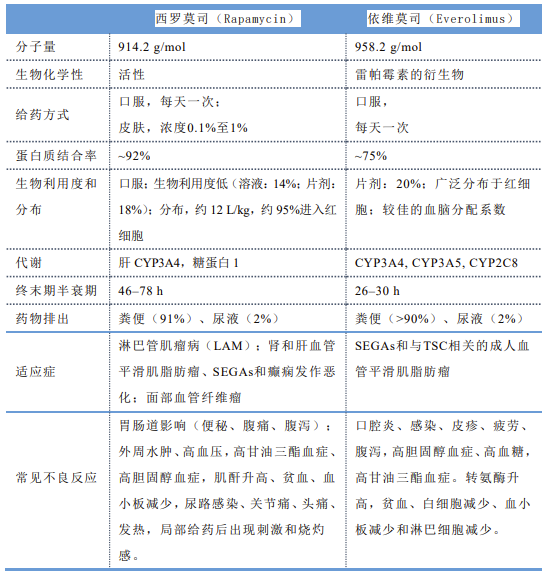
表2 mTOR抑制剂用于治疗TSC
TSC症状分类下的特别说明
皮肤和牙齿
以黑色素脱失斑为代表的皮肤症状是TSC患者最常见临床表现,约发生在90–100%的TSC患者中,常在婴幼儿期显现,可作为TSC发病的提示;成年后减轻,灰发症也属于色素脱失斑的一种。面部血管纤维瘤是血管和结缔组织的错构瘤结节,约发生于75%的病例,以2-5岁发病居多,在青春期内纤维瘤变多变大,严重影响患者外形。25%的TSC患者的前额或其他颅面区域可能出现纤维化斑。其他皮肤还包括甲状纤维瘤、浅绿色斑块、多色纸屑样斑块、牙釉质凹陷和口内纤维瘤。 在治疗皮肤病方面,激光消融、手术切除和移植手术可用于治疗面部血管纤维瘤。面对较高的龋齿风险,可对牙釉质缺陷进行修复。如若口腔纤维瘤干扰到口腔卫生,应手术切除。西罗莫司可作为局部治疗,少数病例报告了在面部血管纤维瘤中使用该药物的获益,持续改善红斑、皮肤损伤。最近一项研究在面部血管纤维瘤患者中,比较了不同剂量的西罗莫司相比安慰剂的疗效显著,以0.2%最佳。
眼睛
视网膜错构瘤约发生在30-50%的TSC患者中,呈半透明扁平肿瘤或白色结节性肿块,被认为是TSC的有效标志物,尤其适用于幼儿的诊断。39%的患者可能出现视网膜色素散点样缺失。TSC诊断时需要进行全面的眼科检查,建议每年一次。尽管眼睛上有这些症状,但如果没影响到眼睛功能,就无需特别治疗。
心脏
心脏横纹肌瘤是在妊娠第20-30周时胎儿及新生儿期可显现的症状,直径约为3-25mm,通常位于心室内;患儿多无症状,随着年龄的增长有机会退化掉;但它们可能与心脏流出道阻塞、心力衰竭、扩张型心肌病、心律失常有关,是TSC婴儿和10岁以下儿童最常见的死亡原因。对于儿童患者,尤其是3岁以下的儿童,应行超声心动图和心电图检查;并在心脏横纹肌瘤消退之前,每1-3年进行一次超声心动图随访,每3-5年进行心电图检查。对无症状的成人患者,不需要超声心动图,但建议用心电图监测。目前,还没有批准的药物治疗这种疾病,重症患者可行手术。
中枢神经系统
TSC的主要神经表现为癫痫,影响约85%的患者。最近的研究发现,TSC1突变型患者的癫痫通常并不严重,智商多数正常。患者可能在儿童期即有难治愈的皮疹。婴儿痉挛症是TSC早期发作的主要类型,这类患者在后续更可能存在神经发育异常或认知障碍。最常见的中枢神经系统病变包括皮质结节、室管膜下结节(SENs)和可扩展到心室的SEGA。SENs见于80%的TSC患者中,通常无症状;而SEGA发生于5-15%的TSC患者中,会导致脑室扩大和脑积水,死亡率较高。TSC患者的神经认知和行为障碍包括攻击性行为、自闭症谱系障碍、智力残疾、精神障碍、神经心理缺陷以及接受学校教育和正常职业的困难,约影响40-50%的病例,不同个体间的症状表现和严重度存在较大差异。 对中枢神经系统症状的治疗,建议对有症状的SEGA行手术切除,或可能需行脑脊液分流。对于生长但无症状的SEGA,手术切除或使用mTOR抑制剂的药物治疗均可显效。依维莫司适用于治疗无法手术而需干预的SEGA患者。氨己烯酸片(Vigabatrin)是γ-氨基丁酸(GABA)转氨酶抑制剂,可调节mTOR的过度激活,是局灶性癫痫和/或婴儿痉挛的首选药物。二线治疗可选择促肾上腺皮质激素(ACTH)或类似物。癫痫手术、生酮饮食或迷走神经刺激可用于难治性患者。西罗莫司和依维莫司均能降低TSC相关难治性癫痫的发作频率。
肺部
肺淋巴管平滑肌瘤病(PLAM)是一种与TSC2基因突变相关的肿瘤性肺病,主要影响育龄妇女,可引起弥漫性囊性组织重塑和进行性呼吸衰竭。早期表现为咳嗽、进行性用力呼吸困难和气胸。多灶性小结节样肺细胞增生和透明细胞瘤是肺部受累的罕见表现。18岁及以上的女性TSC患者可基于肺功能测试、6分钟步行测试、高分辨率胸部CT和血管内皮生长因子-D(VEGF-D)水平监测LAM进展。PLAM通常是全身性和进行性的,除了肺移植,尚无法治愈。西罗莫司现已在美国、日本、韩国、巴西和俄罗斯等获批用于治疗中重度LAM,稳定或改善肺功能,降低血清VEGF-D水平。
肾脏
肾血管平滑肌脂肪瘤是TSC患者另一种常见症状,影响80%的患者,平均发病年龄为43岁;大多数无症状,却是TSC相关发病率和死亡率的最常见原因之一。与普通人群相比,TSC患者发生多发性肾囊肿几率也更高。所有患者在诊断时都应进行腹部影响学检测,MRI是监测肾功能的首选方式。依维莫司被批准用于治疗TSC相关血管平滑肌脂肪瘤。相关指南推荐将mTOR抑制剂作为无症状、>3 cm肾血管平滑肌脂肪瘤的一线治疗。
总结与展望
现代医学研究与临床理念的发展使TSC的诊断、管理越来越趋于整合,多学科协作势在必行。mTOR抑制剂用于治疗SEGA、血管平滑肌脂肪瘤和LAM的获批,及其对难治性癫痫和其他TSC症状的改善作用,代表了TSC治疗进展。雷帕霉素是首个上市的mTOR抑制剂,于1999年在美国获批,2007年在中国获批。雷帕霉素及其类似物因作用于mTOR,对mTORC1和mTORC2的抑制并无差别,毒副作用明显,易产生耐药性,后续尚需优化mTOR抑制剂的使用。二代mTOR选择性抑制剂,如 Torkinib,增强了对下游靶点抑制、蛋白质翻译控制在TORC1和TORC2之间的区分。再有基因疗法、免疫抑制疗法在TSC上的应用也正在加紧研究,与其它罕见病领域一样,当前的发展仍有太多待解的难题,但更远处曙光已现。