
入选《中国地中海贫血蓝皮书(2020)》疗法
β-地中海贫血是一种遗传性溶血性疾病,由于功能性β-珠蛋白严重缺乏,相当一部分患者需定期输血才能存活,从而导致输血依赖性地中海贫血。中国内地β-地中海贫血基因携带者约3000万人,主要分布在我国的广东、广西、福建、云南、贵州、四川、海南等地,重型和中间型β-地中海贫血患者人数在30万左右,且以每年约10%的速度递增。造血干细胞移植是唯一可以根治β地中海贫血的方法,但费用昂贵,且配型极其困难,仅有少部分患者能获得移植。
邦耀生物BRL-101拟定的主要适应症为β-地中海贫血(地贫),是基于邦耀生物自主研发的造血干细胞平台(ModiHSC®)开发的基因治疗产品,利用基因编辑系统对患者的造血干细胞进行基因修饰,修饰后的造血干细胞回输到患者体内;通过自我更新和分化重建修饰细胞群体,达到治疗血液系统疾病的目的。
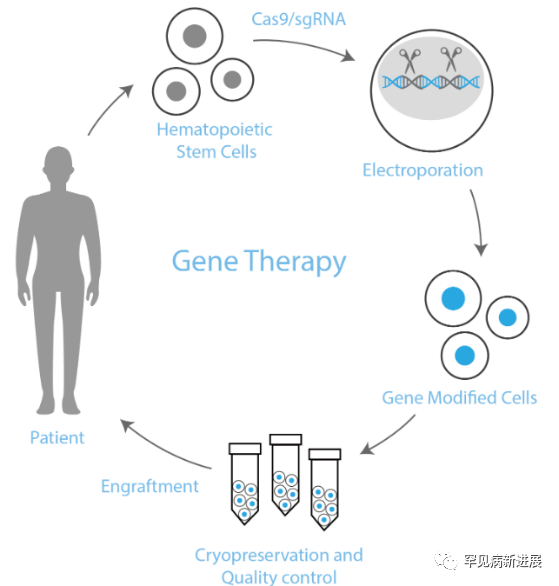
基因疗法的出现给患者带来了希望,最大的优势是不需要捐赠,不需要异体移植,有望一次治疗达到永久性的“治愈”,取代传统方案。而造血干细胞基因疗法更被认为靶向性好、安全性高、作用范围广、治疗效果显著。《中国地中海贫血蓝皮书(2020)》全面调研分析了中国地中海贫血预防、治疗、医疗保障和救助、社会支持等情况,旨在利于国家各省市对后续地贫防治工作,利于社会对地贫群体有更深入的认知;其中在治疗方法部分,即特别收录入邦耀生物在地贫领域的这一突出性成果。
Nature Medicine发表临床试验初步报告
作为首个发表于顶级学术期刊的基于CRISPR基因编辑治疗β0/β0型重度地贫的临床研究,文章公布了详细的临床数据,全面地解读了BRL-101治疗患者的疗效和安全性特征。湘雅医院血液科付斌副主任医师为论文共同第一作者和共同通讯作者,湘雅医院为论文共同通讯及共同第一单位。

该研究基于两名儿童患者的治疗,将基因编辑的自体造血干祖细胞(HSPCs)移植入患者体内,受治患儿的胎儿血红蛋白分别从基线时的2.55g/L、1.75g/L分别上升至最近一次访视的149g/L和139g/L,总血红蛋白含量也分别达到了152g/L和140g/L,且在治疗后都实现了脱离输血依赖超过16个月(脱离输血依赖的定义为:未输血的情况下总血红蛋白达到或超过90g/L)。在整个治疗过程中,清髓预处理相关毒性较轻,未发生严重的感染,并分别于移植后52 天和40 天出院。并且,在近两年的随访期内,没有观察到异常的克隆扩增现象。同时,研发人员对经基因编辑后重建的PBMCs进行了单细胞RNA测序,全面分析由未编辑或编辑的HSPC重组的血液谱系的转录组,表明BCL11A红系特异增强子编辑不会导致非红细胞的显著转录变化,不会影响B细胞以及DC细胞的发育和功能相关基因的表达,这些结果均显示该疗法没有明显的副作用。
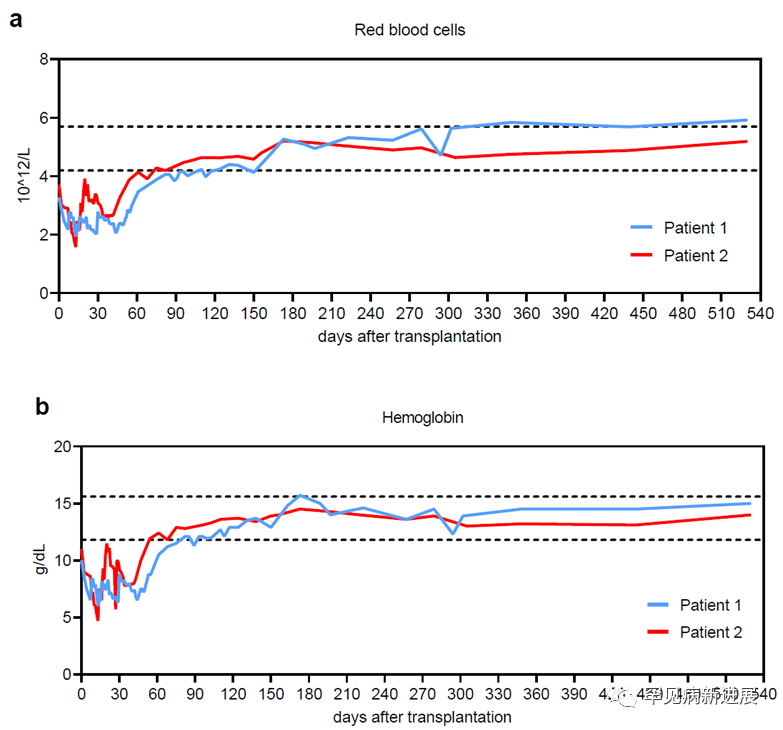
移植后红细胞和总体血红蛋白变化趋势
本项研究被国际认可,不仅为国内基因治疗领域的基础和临床研究提供了成功案例,也有助于促进大众对基因治疗的科学认识,有助于推动国内对基因治疗研究的监管,为后续基因治疗领域的健康发展奠定了积极的良好基础。
医企联心,共铸患者希望
自2020年7月以来,邦耀生物和中南大学湘雅医院血液科付斌副主任医师及中国人民解放军联勤保障部队第九二三医院张新华主任合作,基因治疗多例β地贫患者已治愈出院。其中湘雅的2例患者摆脱输血依赖已超2年,这是亚洲首次通过基因编辑技术治疗地贫,也是全世界首次通过CRISPR基因编辑技术治疗β0/β0型重度地贫的成功案例。
付斌副主任医师已带领学组在重型地中海贫血造血干细胞移植领域开展了多年的工作。他曾介绍,如果说输血是将“果实”输入到患者体内,通过补充正常的血液来纠正贫血。那么造血干细胞移植就是把“种子”移入进去,让正常的造血干细胞在体内取而代之、生根发芽,从而彻底摆脱输血。相比美国之前开展的β0/β+型基因治疗临床试验,β0/β0的治疗难度更大。β0/β0型患者由于两个β基因均完全不表达,要达到临床疗效,对激活的效率和深度(有效基因所占的百分比)要求更高。

湘雅医院网站新闻对该研究的阶段性成果均发布了要闻报道,还在去年全省“两会”期间,参与提交了《关于我省地中海贫血防治整体策略的提案》,共同推动和倡导社会各界积极关注和参与地中海贫血的防治工作。这些既体现了医、企合力,又为全社会关注地贫儿特殊群体提供了榜样,开拓着治愈性希望。BRL-101自体造血干祖细胞注射液获批临床后,仍有大量繁重的研究工作需要开展,为编辑生命的希望,期待医、企、患终将协奏交响乐章。