
图片来源:摄图网
勃林格殷格翰(Boehringer Ingelheim)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一份积极审查意见,建议有条件批准Spevigo(spesolimab,司柏索利单抗):用于治疗成人泛发性脓疱型银屑病(GPP)发作。GPP是一种罕见、危及生命的中性粒细胞性皮肤病,其特征是疼痛、无菌脓泡,可突然出现在全身。尽管名称上有银屑病,但GPP与更常见的斑块型银屑病有很大不同。GPP发作是不可预测的,通常需要急救,并可能导致严重的危及生命的并发症,如休克和多系统器官衰竭。
2022年9月初,Spevigo已获得美国FDA批准,用于治疗成人GPP发作。在美国,Spevigo是该病的首个且唯一的治疗方案。Spevigo专门靶向IL-36通路,这是GPP发病机制的核心。
Spevigo是一种新型人源化选择性抗体,可阻断白细胞介素-36受体(IL-36R)的激活,这是免疫系统内的一种信号通路,参与多种自身免疫性疾病的发病机制,包括GPP。Spevigo是第一个专门靶向IL-36通路治疗GPP发作的药物,已在一项随机、安慰剂对照临床试验中进行了评估。此外,spesolimab也正被研究,用于预防GPP发作和治疗其他中性粒细胞皮肤病,如掌跖脓疱病(PPP)和化脓性汗腺炎(HS)。
GPP是一种罕见的、异质性的、可能危及生命的中性粒细胞性皮肤病,临床上与斑块型银屑病不同。GPP是由中性粒细胞(一种白细胞)在皮肤中积聚引起的,导致全身疼痛、无菌脓疱。GPP的临床病程不同,一些患者有复发性疾病并伴有反复发作(flare),而另一些患者有持续性疾病并伴有间歇性发作。虽然GPP发作的严重程度可能会有所不同,但如果不进行治疗,可能会因败血症和多系统器官衰竭等并发症而危及生命。这是一种慢性、系统性疾病,会对患者的生活质量和医疗负担有重大影响。GPP在不同地理区域的流行程度不同,受影响的女性多于男性。
GPP的特征是疼痛、无菌脓疱(非感染性脓疱)的广泛爆发,炎症还可影响身体其他部位,并可导致感染或其他可能危及生命的器官并发症。GPP治疗方面,对可以迅速和完全解决GPP发作症状、防止其再次发生、具有可接受安全性的有效药物存在着非常高的未满足医疗需求。GPP发作会极大地影响患者的生活质量,并可能导致住院治疗,出现危及生命的并发症,如心力衰竭、肾功能衰竭、败血症甚至死亡。基于斑块型银屑病患者的临床治疗经验,包括生物制剂在内的免疫调节疗法已被应用于GPP的治疗。然而,关于这些疗法治疗GPP的有效性和安全性的证据有限。
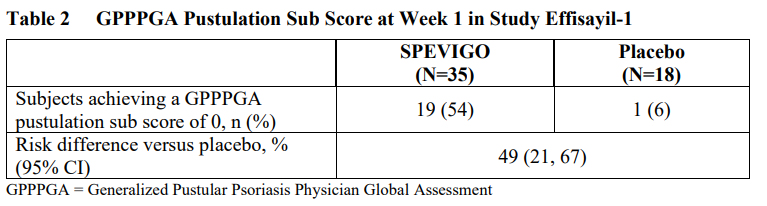
EFFISAYIL-1临床试验数据(图片来源:Spevigo美国处方信息)
CHMP对spesolimab的积极审查意见,基于关键性2期EFFISAYIL-1临床试验(NCT03782792)的结果。这是一项为期12周的多中心、双盲、随机、安慰剂对照试验,在经历GPP发作的患者中开展,大多数患者在试验开始时脓疱密度高或非常高,且生活质量受损。研究评估了spesolimab(单剂量900mg spesolimab静脉输注,如果症状在第8天持续存在,可选择输注第2剂)相对于安慰剂的疗效、安全性和耐受性。
结果显示,spesolimab在清除脓疱方面疗效显著优于安慰剂:治疗一周后,spesolimab治疗组有54%的患者没有可见的脓疱,安慰剂组仅为6%。一周后,spesolimab组有66%、安慰剂有56%的患者发生不良事件。spesolimab组和安慰剂组分别有17%和6%的患者报告感染(在第一周)。在接受spesolimab治疗的患者中,有6%发生严重不良事件(在第一周)。
勃林格殷格翰董事会成员、人用药负责人Carinne Brouillon表示:“CHMP的积极建议,认可了spesolimab作为一种新颖靶向单抗的潜力,可以治疗GPP的根本原因。spesolima的加速开发彰显了我们继续致力于为医疗需求未得到满足的人群开发更快、更新颖治疗方法。”