
2022年10月26日~28日,第38届欧洲多发性硬化症治疗和研究协会(ECTRIMS)大会在荷兰阿姆斯特丹举行。视神经脊髓炎谱系疾病(Neuromyelitis optica spectrum disorders,简称NMOSD)作为一种罕见的高复发、高致残性中枢神经系统自身免疫性疾病,也是本次大会的热点议题之一,相关研究成果涉及NMOSD的流行病学、发病机制以及治疗进展等。
作为全球首个获批用于NMOSD治疗的B细胞耗竭剂,伊奈利珠单抗(inebilizumab)临床疗效和安全性已在大型随机对照III期临床研究中得到证实。2019年5月,翰森制药获得伊奈利珠单抗在中国的开发和商业化权利,并于2022年3月宣布获中国国家药品监督管理局上市批准,用于抗水通道蛋白4(AQP4)抗体阳性的NMOSD成人患者的治疗,从而为国内NMOSD患者带来希望。本次大会共发布了四项伊奈利珠单抗的最新研究,进一步为伊奈利珠单抗的临床应用提供了可靠的证据支持。
1.P007:间接比较分析表明,伊奈利珠单抗预防NMOSD发作相比萨特利珠单抗更具优势[1]
德国研究者F. Paul等人对两种治疗AQP4-IgG阳性NMOSD的生物制剂——伊奈利珠单抗(靶向CD19的B细胞耗竭剂)和萨特利珠单抗(IL-6受体拮抗剂)单药治疗的注册临床试验进行了匹配调整的间接比较(MAIC)分析,旨在为临床治疗决策提供参考依据。
本次分析纳入的数据来源是伊奈利珠单抗的N-MOmentum研究(NCT02200770)和萨特利珠单抗的SAkuraStar研究(NCT02073279),这两个临床研究均采用安慰剂对照,并采用类似的评估和终点,主要研究终点均是至首次判定发作的时间。
结果显示,两个研究均达到了主要疗效终点,与安慰剂组比,伊奈利珠单抗和萨特利珠单抗治疗的未调整风险比(HR)分别为0.227和0.261。经MAIC分析后,伊奈利珠单抗治疗组的HR从0.227改善到0.174,伊奈利珠单抗与萨特利珠单抗的相对风险比为0.67,这意味着与萨特利珠单抗相比,伊奈利珠单抗治疗后的复发风险降低33%。即接受萨特利珠单抗治疗的患者每发作100次,伊奈利珠单抗治疗的患者预计仅发作67次(表1)。
表1.主要疗效终点:AQP4+患者的至首次判定发作时间风险比(HR,95%CI)
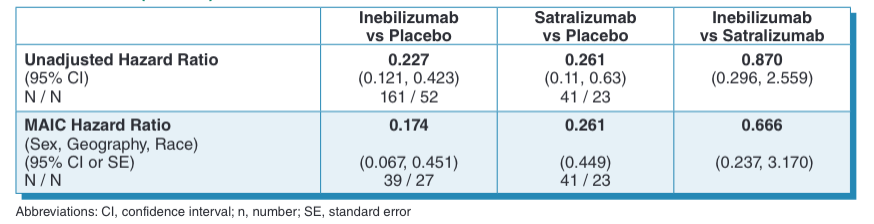
在对性别、地理、种族、既往发作等因素进行多重敏感性分析评估后,进一步证实了该结果的有效性(伊奈利珠单抗相比萨特利珠单抗的复发风险至少下降20%)。
研究认为,尽管这种间接比较具有一些局限性,但结果提示伊奈利珠单抗在预防NMOSD发作方面相比萨特利珠单抗具有疗效优势。
NMOSD复发时,患者外周血B细胞亚群数量和AQP4抗体滴度可以反映发作的严重程度及预后。为此,来自美国梅奥诊所的S.J.Pittock等人组成的国际研究小组评估了N-MOmentum研究中受试者外周血B细胞亚群数量和AQP4-IgG滴度的变化与NMOSD发作之间的关系。
N-MOmentum研究中,受试者们被随机分配至治疗组和安慰剂组,在第1天和第15天分别注射伊奈利珠单抗300mg和安慰剂(随机对照期),随后每6个月注射一次(开放期),观察两年。每次随访时,抽取外周血,测定CD20+B细胞和CD27+记忆B细胞的绝对计数、浆细胞基因表达量和AQP4-IgG滴度。
研究结果显示,安慰剂组的CD20+B细胞和CD27+记忆B细胞在复发时相比前次就诊时显著增加(p<0.05),前次就诊时的浆细胞基因表达量相比基线也有明显增加(p<0.01)。在发作期间,20%(4/20)的患者CD20+B细胞、16%(3/19)的患者记忆B细胞和57%(12/21)的患者浆细胞表达量相比基线增加2倍以上。
相比安慰剂,伊奈利珠单抗显示出快速而持久的浆细胞耗竭作用(图 1A)。伊奈利珠单抗组发作时和前次就诊时的浆细胞特征基因表达量自基线的中位倍数变化值分别为0.041(0.017-0.11)和0.048(0.034-0.082)(图 1B)。
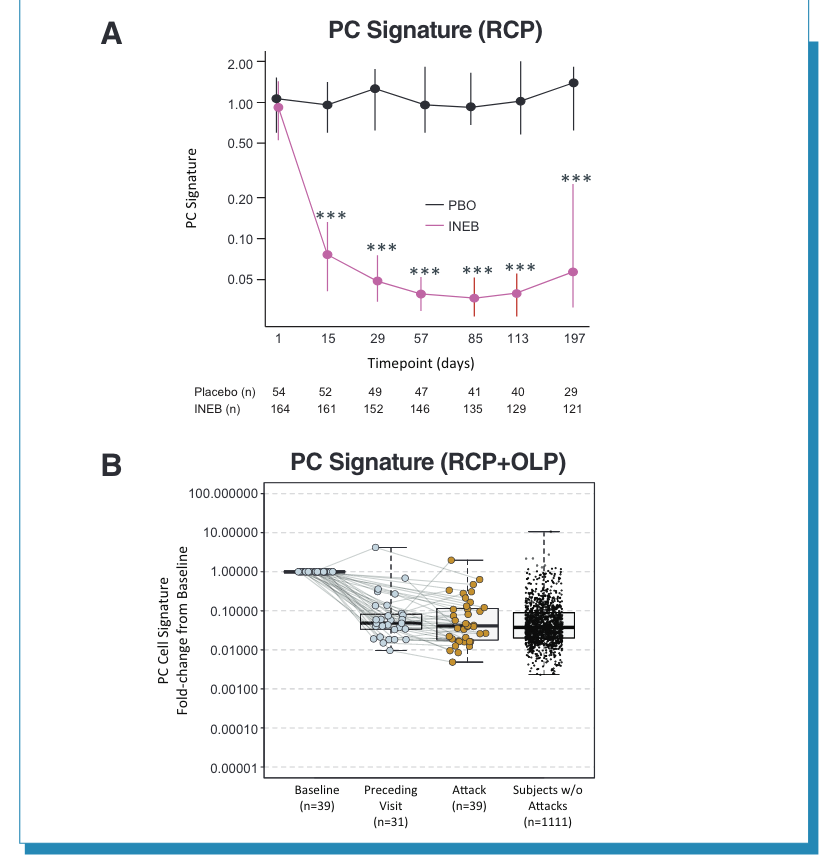
伊奈利珠单抗组所有B细胞亚群数量均显著降低,且发作时的任何B细胞亚群相比前次就诊时均无明显升高。至随机对照期结束,安慰剂组和伊奈利珠单抗组AQP4-IgG下降⩾2倍的患者比例分别为18%和37%(P=0.014),下降⩾8倍的患者比例分别为0%和11%(P=0.008)(图 2A)。
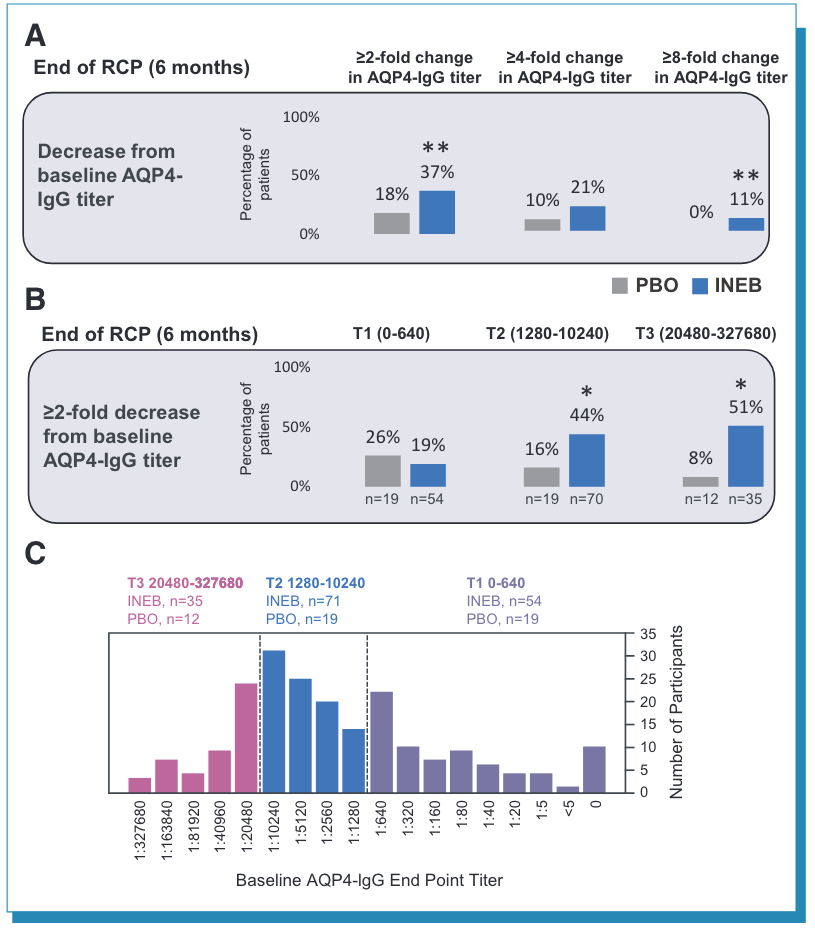
图 2. (A)安慰剂组(n=50)和伊奈利珠单抗组(n=159)AQP4-IgG滴度降低≥2倍,≥4倍以及≥8倍的受试者占比;(B)AQP4-IgG滴度降低≥2倍三分位数分层,各分层受试者占比;(C)受试者基线AQP4-IgG滴度情况细分。
研究表明,NMOSD发作时B细胞亚群水平升高主要出现在安慰剂组,而非伊奈利珠单抗组,尤其是浆细胞亚群,且部分患者在接受伊奈利珠单抗治疗后出现AQP4-IgG滴度下降。研究提示伊奈利珠单抗与浆母细胞/浆细胞耗竭及AQP4-IgG下降具有相关性。
去岩藻糖基化的单克隆抗体被设计用于增强对Fc受体III-A(FCGR3A)的亲和力,并使抗体依赖性细胞毒性反应(ADCC)最大化,从而增强药效,而既往研究发现FCGR3A的F176V多态性(rs396991)的F等位基因与利妥昔单抗在NMOSD中的IgG结合亲和力降低和疗效下降有关。
因此,德国研究者O.Aktas等人组成的一个国际研究小组对N-MOmentum研究(伊奈利珠单抗治疗NMOSD的双盲随机安慰剂对照2/3期试验)进行了一项事后分析,以探索该多态位点(rs396991)是否会影响伊奈利珠单抗的药效。该研究总共纳入了142例参与者(伊奈利珠单抗组104例,安慰剂组38例),记录其临床信息并根据其基因多态位点特征进行分组。
结果显示,F等位基因组(F/F)患者(n=68)与V等位基因组(V/V或V/F)患者(n=74)在基线人口学特征或病程上无显著差异。V等位基因组 vs F等位基因组的CD20+B细胞耗竭情况类似[至随机对照期结束时:0.6(0.1–3.2) vs 1.3(0.5–4.2)细胞/μL],且在整个研究过程中两组的B细胞耗竭情况均保持稳定;同样,两组在疾病复发风险[OR0.94(0.39,2.24)]和EDSS评分恶化[OR1.55(0.54,4.70)]方面也没有差异(表2)。
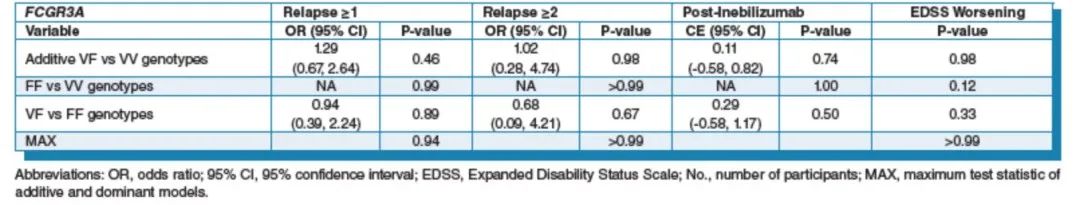
此外,接受伊奈利珠单抗治疗患者的年化发作率在三种多态基因型中均较低,分别为V/V0%、V/F4%和F/F3%,组间均没有显著性差异。该结果表明,无论NMOSD患者是否存在FCGR3A基因多态性,伊奈利珠单抗均能降低复发风险。
N-MOmentum研究(NCT02200770)是一项多中心、双盲、随机、安慰剂对照的2/3期研究,旨在评价伊奈利珠单抗治疗NMOSD成人患者的有效性和安全性。该试验期间禁止患者使用免疫抑制剂,但是许多患者在接受伊奈利珠单抗治疗前,很可能已接受过免疫抑制剂的治疗。因此,评估此类患者使用伊奈利珠单抗的有效性和安全性具有重要的临床意义。
德国研究者F.Paul等人组成的一个国际研究小组开展了一项事后分析,根据有无免疫抑制剂治疗史对N-MOmentum研究中接受伊奈利珠单抗治疗的AQP4+参与者进行分组,评估伊奈利珠单抗在这两类患者中的长期治疗结局。
结果显示,在整个研究期间,接受伊奈利珠单抗治疗的参与者中,有94例既往接受过硫唑嘌呤/吗替麦考酚酯(AZA/MMF)治疗,103例未接受过免疫抑制治疗。既往接受过AZA/MMF治疗的患者年化复发率为11%,年化NMOSD相关住院率为15%,而无免疫抑制剂治疗史的患者则分别为8%和12%。无论既往是否接受过免疫抑制剂治疗,伊奈利珠单抗长期治疗期间所有患者均维持较低的发作几率(图 3)。
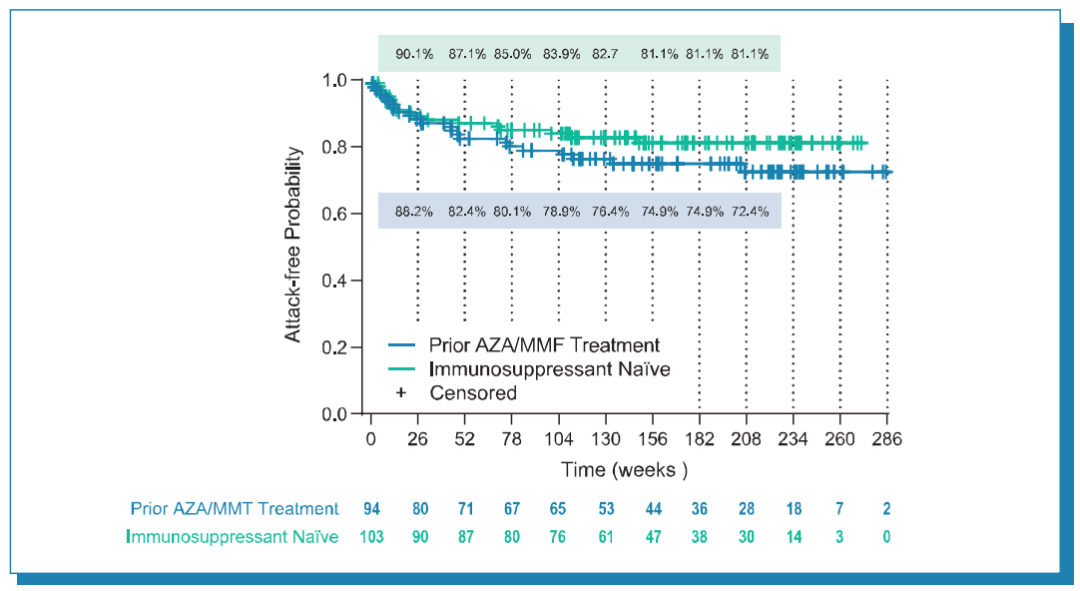
安全性方面,既往接受过AZA/MMF治疗的患者中,出现⩾1个伊奈利珠单抗相关的治疗期间不良事件(TEAE)的患者比例为30.9%(29/94),无免疫抑制剂治疗史的患者中为46.6%(48/103),且大多数不良事件与感染相关。
研究表明,既往接受过AZA/MMF传统免疫抑制剂治疗的AQP4+NMOSD患者使用伊奈利珠单抗长期治疗,其疗效与安全性与无免疫抑制剂治疗史的患者没有明显差别。
N-MOmentum研究为伊奈利珠单抗在国内外的获批上市及临床应用奠定了基础,本次大会公布的四项新研究,揭示了伊奈利珠单抗的显著疗效可能与耗竭浆细胞及降低AQP4-IgG滴度有关,并进一步证实了靶向CD19的伊奈利珠单抗相比其它靶向药物(IL-6受体拮抗剂)在NMOSD中的治疗优势,且无论患者既往是否接受过传统免疫抑制剂治疗,以及是否存在FCGR3A基因多态性,都能够获益于伊奈利珠单抗治疗。期待未来有更多的伊奈利珠单抗研究成果,以改善NMOSD这一罕见病患者群体的疾病管理和生存质量。
参考文献:
1. F.Paul, et al. Efficacy comparison of time to first adjudicated attack with inebilizumab vs satralizumab in NMOSD: a matching-adjusted indirect comparison of monotherapy registrational trials. Multiple Sclerosis Journal 2022; 28: (3S):134
2. S.J.Pittock, et al. Association of B cell subsets and aquaporin-4 antibody titers with disease activity in participants in the N-MOmentum trial receiving inebilizumab treatment. Multiple Sclerosis Journal 2022; 28:(3S):137-8
3. O.Aktas, et al. Inebilizumab reduces attack risk independent of low affinity igG Fc region receptor III-a gene polymorphisms in neuromyelitis optica spectrum disorder. Multiple Sclerosis Journal 2022; 28: (3S):416-7
4. F.Paul,et al.Safety and efficacy of Inebilizumab in AQP4+ NMOSD participants with history of immunosuppression treatment prior to N-MOmentum study. Multiple Sclerosis Journal 2022; 28: (3S):422-3