2022年11月28日,罕见病精准遗传医学领域的领导者Sarepta Therapeutics(纳斯达克代码:SRPT)今天宣布,FDA已经接受了该公司的生物制品许可申请(BLA),以加速批准SRP-9001 (delandistrogene moxeparvovec)用于治疗杜氏肌营养不良患者。SRP-9001已获得FDA的优先审查,PDUFA日期为2023年5月29日。
受到此消息影响,截止北京时间23点,Sarepta Therapeutics股价121美元/股,涨幅6%,目前100亿美元,今年以来股价累计涨幅近50%。

SRP-9001(delandistrogene moxeparvovec)是一种研究性基因疗法,旨在将目的基因递送到肌肉组织,并且有针对性地产生抗肌萎缩蛋白的有效成分。2019年底,Sarepta Therapeutics与Roche达成协议,Roche获得SRP-9001在美国以外地区的独家权利签署协议,并分担SRP-9001的全球开发成本。Sarepta Therapeutics将获得7.5 亿美元现金和 4 亿美元股权的预付款,以及未来可能高达17亿美元的里程碑付款。
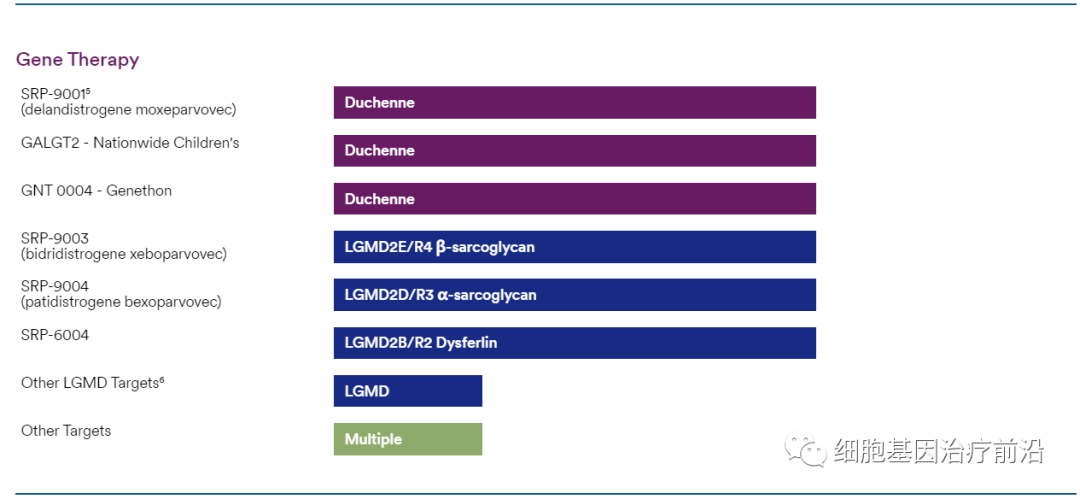
Sarepta的基因治疗和基因编辑管线

杜氏肌营养不良症(DMD)是一种罕见的、致命的神经肌肉遗传病,全球大约每3500—5000名新生男性中就有1人发生。DMD是由编码抗肌萎缩蛋白指令的基因发生改变或突变引起的。DMD的症状通常出现在婴幼儿中。
“我们很高兴地宣布,FDA 已接受 Sarepta 的 SRP-9001 BLA 进行备案和优先审查,”Sarepta Therapeutics 总裁兼首席执行官 Doug Ingram 说,“Duchenne 是一种无情的退化性疾病,并且总是致命的,它每天每时每刻都在剥夺儿童的肌肉和功能。我们提交的 BLA 加速批准,以及 FDA 接受该 BLA 进行备案和审查,是我们努力尽快为 Duchenne 患者带来可能改变生命的基因疗法的一个极其重要的里程碑,我们期待着通过审查过程与 FDA 合作。”
Sarepta 拥有治疗杜氏肌营养不良(DMD)的三款ASO重磅产品——Exondys 51、Vyondys 53和Amondys 45,2022年前三季度实现销售额6.08亿美元(约为43亿人民币),同比增长40%。(1美元 ≈ 7.15人民币)。
此外,辉瑞的DMD基因疗法也有进展。
今年4月份,辉瑞公司宣布,美国FDA已经通知该公司,允许其治疗杜氏肌营养不良(DMD)的基因疗法fordadistrogene movaparvovec的3期临床试验继续进行,这是一款在研静脉注射基因疗法。这个名为CIFFREO的全球性3期临床试验在去年12月因为在1b期临床研究中一名患者出现致命不良事件而暂停;此后辉瑞对临床试验流程进行了修改,满足了监管要求。
参考资料:
https://www.sarepta.com/