11%的单基因遗传疾病是由人类基因中的过早终止密码子(PTC)引起的,其中突变的转录本会生成功能受损的截短蛋白质,从而导致无义突变PTC疾病[1]。近期,我院天然药物及仿生药物国家重点实验室夏青团队基于蛋白质翻译提前终止的机制,应用基因密码子扩展技术中的重要元件,即工程化“tRNA—氨酰tRNA合成酶”正交系统对模型小鼠中致病基因的无义突变进行通读治疗。实验不仅验证了“tRNA—酶”能够在动物体内稳定表达,而且可以精准通读内源性的发病位点,从而能够恢复蛋白的全长表达,缓解疾病的症状。此项研究从突变类型的角度,提出了通用型治疗无义突变的方法,是一种治疗单基因遗传疾病的新策略[2]。为推进这种新型疗法的转化研究,亟需建立动物水平的实验流程和评价标准,为临床前研究的提供坚实基础。

2023年3月17日,夏青团队受邀在Cell子刊STAR Protocols杂志在线发表了题为“Adeno-associated viral delivery of engineered tRNA-enzyme pairs into nonsense mutation mouse models”的实验方案文章(Protocol)。该文章提出了利用工程化“tRNA—酶”正交系统来通读无义突变的位点,通过引入一个非天然氨基酸(UAA)来恢复致病蛋白表达的新型治疗策略。文章详细介绍了如何筛选和优化tRNA-酶正交对以实现有效的 UAA引入,利用腺相关病毒(AAV)载体进行腹腔和肌肉注射的两种递送方式,详细评价了治疗效果。该工作突破了以往只能局限于使用基因治疗和基因编辑逐一进行每个基因的药物研发模式,为今后开创通用型点突变罕见病治疗提供有效工具。
在过去的二十年里,基因密码子扩展技术已经从一个奇妙的想法发展成为一个强大的研究工具,并提供了多种工程化“tRNA—氨酰tRNA合成酶”正交对,与相应的非天然氨基酸[3]。对于疾病蛋白的内源性无义突变,首先需要筛选出能有效通读该突变位点的正交翻译系统。研究团队建立了正交对的优化和筛选体系,在筛选过程中,需要进行以下步骤:(1)tRNA与合成酶文库的合成与UAA的选择;(2)用于筛选的tRNA与合成酶表达载体的构建;(3)检测不同的正交对和对应UAA的各项指标,以确定通读疾病不同无义突变位点的最佳组合;(4)在多种体外模型中验证该系统的有效性。(图1)
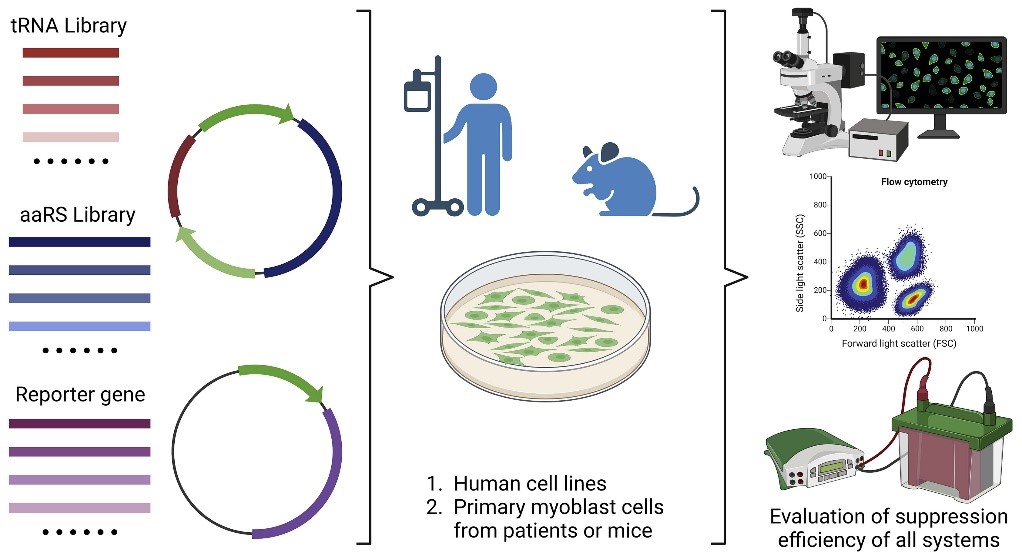
图1 正交系统筛选流程简图
(图源:Zheng Z, et al., STAR Protoc, 2023)
杜氏肌营养不良症(DMD)是一种人类X染色体连锁隐形遗传疾病,其中约10%的病例是由于DMD基因中的无义突变所引起,DMD患者往往表现出进行性肌肉无力,随年龄增长将伴随呼吸障碍和心力衰竭[4]。研究团队利用腺相关病毒(AAV)载体搭载优化和筛选得到的正交系统,分别以腹腔注射和肌肉注射的方式递送至DMD疾病小鼠模型体内,而非天然氨基酸则通过腹腔注射给予。除了监测各组小鼠在治疗过程中的生存率、体重变化(安全性)等基本指标,研究团队还采集了多项数据来评估DMD小鼠的治疗效果,包括(1)分子水平的dystrophin蛋白的表达恢复(金标准,与DMD疾病强相关);(2)细胞水平的肌酸激酶(CK)和乳酸脱氢酶(LDH)的表达;(3)组织水平的小鼠肌肉组织的病理变化和修复情况;(4)行为学水平的握力恢复、小鼠的运动能力和协调性;(5)安全性验证:使用免疫学方法,如淋巴细胞亚群分析和细胞因子检测等,评估小鼠免疫系统的状态和炎症反应。
最后,基于以上评价指标,研究团队观察到治疗组小鼠体内dystrophin蛋白在肌肉、横膈膜和心脏中的表达效率,以及肌肉组织病理状态的修复与肌肉力量明显增加,这代表着利用AAV递送的基因密码子扩展系统可以有效恢复DMD小鼠的肌肉功能,延缓疾病进程,并缓解心脏和呼吸系统的发病症状,表明这种新型疗法有应用于未来临床治疗的巨大潜力。(图2)
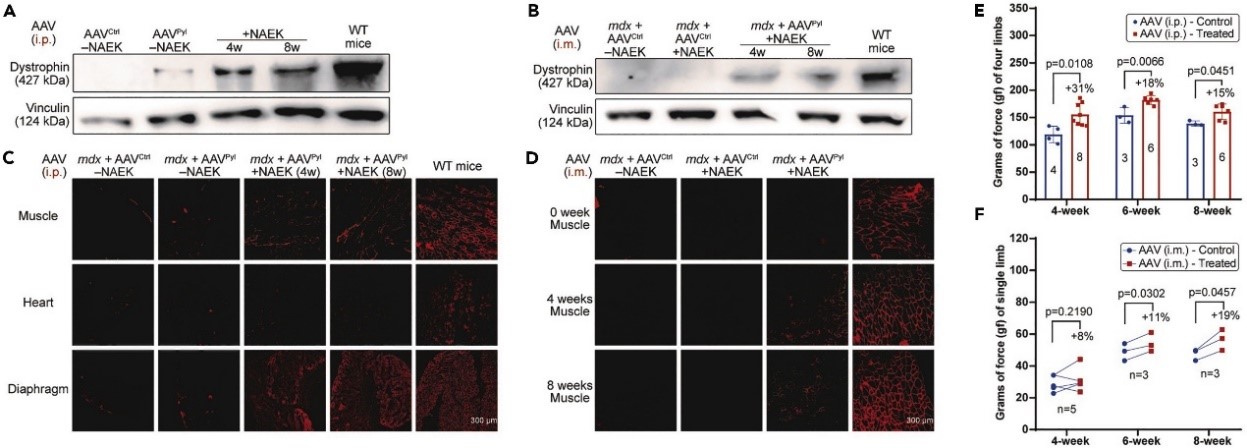
图2 部分评价指标
(图源:Zheng Z, et al., STAR Protoc, 2023, referred to Shi N, et al., Nat. Biomed. Eng, 2021)
【总结与展望】
综上,该文章提供了详尽的实验及评价方法,建立了利用基因密码子扩展技术通读内源性致病的无义突变位点,开创了一种治疗罕见病的新策略。该疗法的核心是制备新型生物正交的蛋白质翻译机器来通读PTC位点并恢复功能性蛋白质的表达,从蛋白质编辑的角度来治疗遗传性疾病。