
True NorthTherapeutics公司,一家开发新型候选产品选择性抑制补体系统以治疗某些罕见疾病的临床阶段生物技术公司,近日宣布:美国食品与药物管理局(FDA)已经授予公司重点候选产品TNT009 治疗自身免疫性溶血性贫血,包括冷凝素病(CAD)的孤儿药地位。
CAD是自身免疫性溶血性贫血的一种形式,患者可用的治疗选择有限。TNT009 目前正在CAD患者中进行1b期临床研究,并于2016年6月宣布了积极的中期结果。2016年2月,TrueNorth公司获得欧洲药物管理局(EMA)授予TNT009的孤儿药地位。
“TNT009获得EMA和FDA的孤儿药地位,是为CAD患者开发急需新治疗选择的重要里程碑”True North公司首席执行官Nancy Stagliano 博士说,“我们期待继续为CAD开发TNT009,并在数据可用时报告额外的1b期临床数据。”
FDA授予的孤儿药地位为那些用于安全有效地诊断、治疗及预防罕见疾病(美国患者人数少于20万)的新型药物和生物制剂提供了特殊的地位。孤儿药地位为药物开发商提供一定的激励措施,可能包括临床研究费用税务抵免和处方药用户费用豁免。获得FDA孤儿药地位的产品如果后来得到FDA批准为第一种治疗相应疾病的疗法,将拥有孤儿药产品市场独占权。
关于冷凝集素病(CAD)
CAD是一种自身免疫性溶血性贫血,这种病中自身抗体瞄准和破坏红细胞,造成贫血、疲劳并潜在形成致命血栓。原发性CAD的发病率大约为每百万人中16例。目前该病可用的治疗选择有限,许多接受治疗的患者依然存在中到重度贫血。True North公司赞助了一个CAD和其他自身免疫性溶血性贫血患者的注册登记项目,名为COMPASS Registry,致力于推进对这些疾病更深入的理解,与患者更好的接洽,以及支持临床试验招募。
关于TNT009
TNT009是一种首创单克隆抗体,通过以C1s为靶点选择性抑制经典补体通路。C1s是一种丝氨酸蛋白酶,存在于免疫系统经典补体通路中的C1-复合物中。TNT009因而可以防止涉及细胞吞噬作用、炎症和细胞溶菌作用的下游疾病过程。由于独特的作用机制和高靶点特异性,TNT009能够在选择性抑制经典补体通路中疾病过程的同时,维持由补体旁路和补体凝集素通路提供的重要免疫监控。TNT009目前正在进行治疗冷凝集素病(CAD)的临床开发,CAD是一种罕见的血液科疾病。由于大量其他疾病已知存在可以被TNT009解决的基础机制,TNT009治疗其他适应症的潜力是明显的。
关于True North Therapeutics
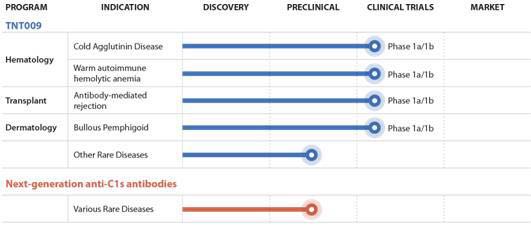
True North Therapeutics公司位于加州南旧金山,是一家临床阶段生物制药公司,关注于补体介导疾病首创候选产品的发现、开发和商业化。公司的优先候选产品TNT009被设计为选择性抑制经典补体通路中的一个靶点。True North公司抗体药物的开发重点是治疗某些由补体系统介导的血液科、移植和皮肤科罕见病。
原文链接:
--------------------
校审/曹文东、夏蓓
本文由中国罕见病网编译,转载请注明出处。