
中国的罕见病患者长期缺乏有效药物治疗,罕见病临床试验开展困难是其中一个重要原因。2021年12月31日,国家药监局药品审评中心发布了《罕见疾病药物临床研发技术指导原则》。国内罕见病药物临床开发可望加速。
重庆医科大学药学院药品政策与评价研究中心联合蔻德罕见病中心发起了一项关于中国罕见病患者/家属对罕见病临床试验的认知、态度与实践情况的调查研究。目的是基于以罕见病患者为中心的理念,了解罕见病患者对临床试验认知度和参与度,以及罕见病患者参与临床试验的关切与障碍,为提高罕见病患者临床试验素养与参与度,促进罕见病治疗药物的临床开发,满足罕见病患者临床需求提供政策建议与决策参考。
本调查从2021年11月1到2021年11月30日,以罕见病患者或家属为调查对象,通过各罕见病组织定向发布以及罕见病患者滚雪球发布相结合的方式,共收集到问卷1573份,纳入有效问卷1498份。1498份有效问卷中,62.5%由他人代答,37.5%由患者本人填写。
中国罕见病患者参与临床试验的现状调查报告摘要(文末可获取完整版报告)
一.被调查患者的基本信息
· 共涵盖了142种罕见疾病
· 18岁及以下的被调查患者占54.9%
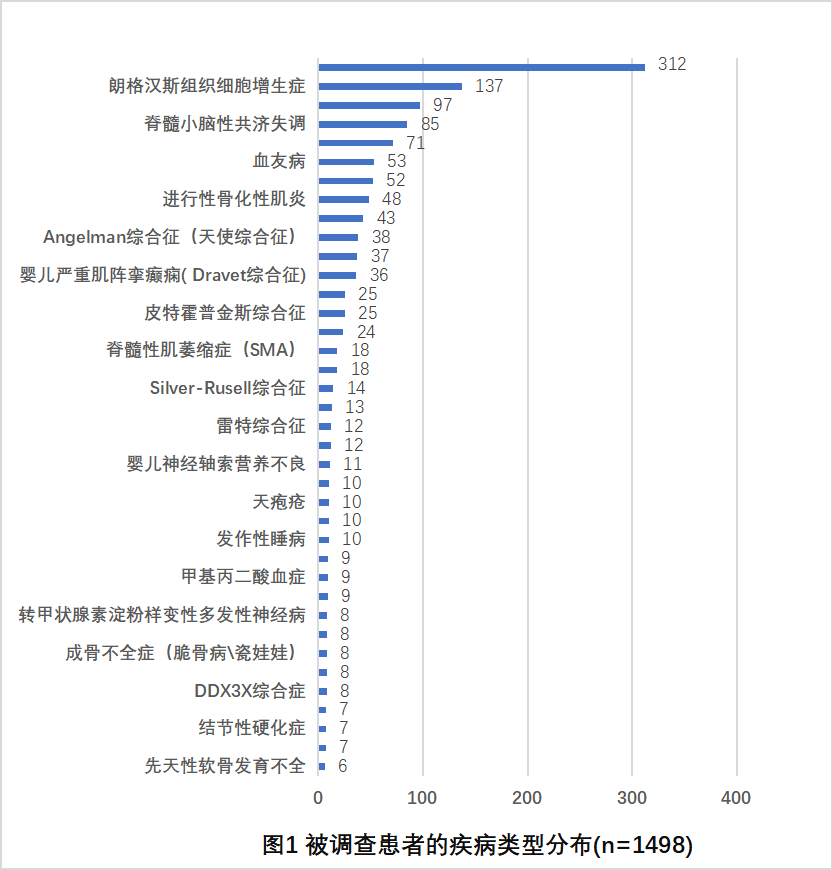
疾病类型分布(图1)
二.被调查者对临床试验的认知现状
· 75.5%的被调查者听说过临床试验
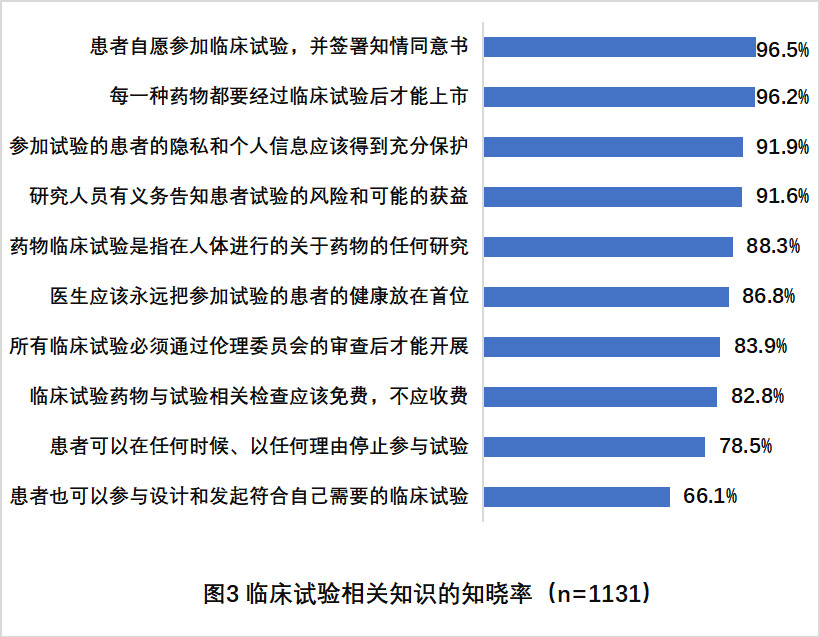
· 33.9%的被调查者不知道“患者可以参与设计和发起临床试验”
· 21.5%的被调查者不知道“患者可以在任何时候以任何理由停止参与试验”
· 17.2%的被调查者不知道“临床试验药物与相关检查应该免费,不应收费”
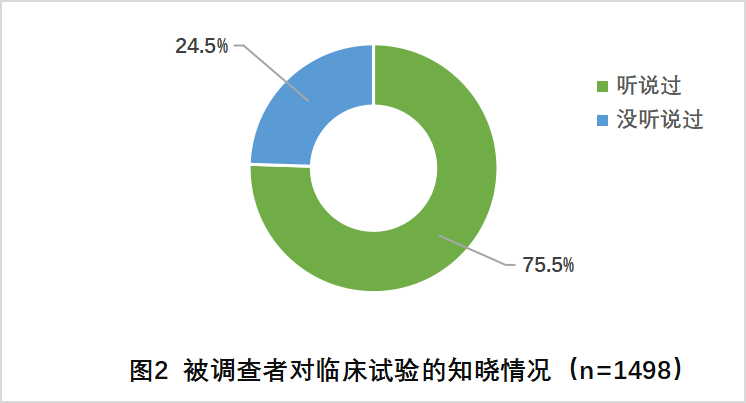
以下调查数据均针对听说过临床试验的1131名被调查者展开。
三. 被调查者对临床试验的实践情况
· 62.0%的被调查者通过网络社交软件或新媒体了解到临床试验信息
· 63.6%的被调查者主动寻找过临床试验信息
· 仅有8.9%的被调查者参加过临床试验
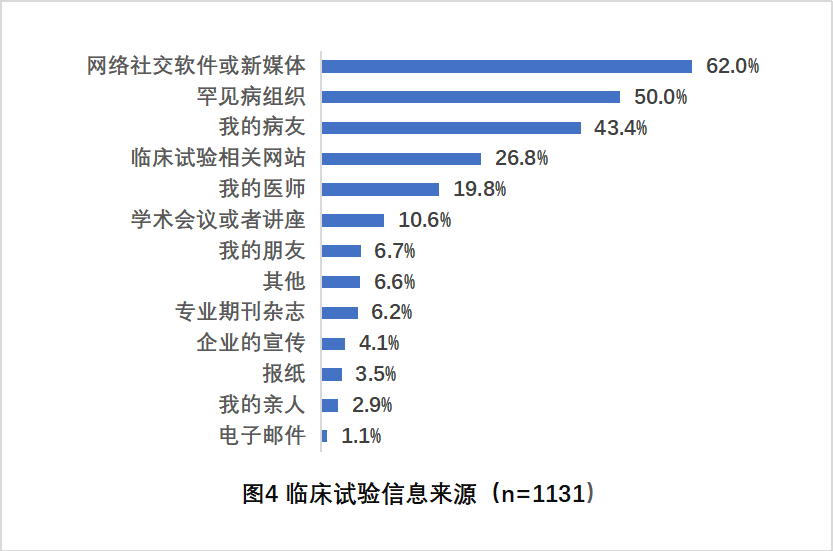
被调查者的临床试验信息来源 (图4)
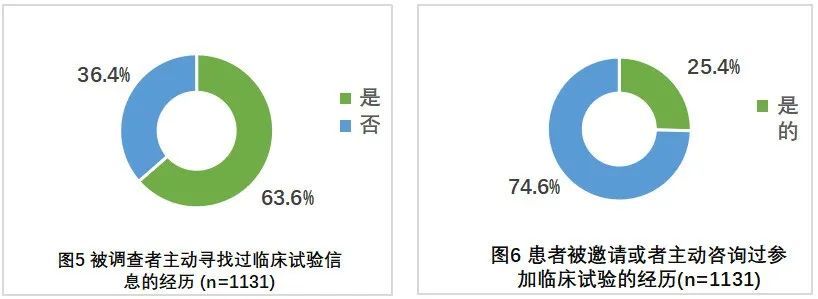

被调查者临床试验相关实践情况(图5-图8)
四. 被调查者对参加临床试验的态度
· 84.8%的被调查者愿意参加罕见病临床试验
· 在促进参加罕见病临床试验的因素方面,88.2%的被调查者选择“参加试验可能治愈疾病”的同意率最高,其次为“希望得到医生更多的关注和医疗服务”和“参加试验可能减轻主要症状”,分别为92.1%和91.5%
· 在阻碍参加罕见病临床试验的因素方面,57.3%的被调查者选择“没有获得临床试验信息的来源或者途径”,其次为“担心试验药物的安全性(副作用,病情加重)”和“担心试验药物的有效性(治疗获益,纳入安慰剂组)”,分别为54.4%和49.1%
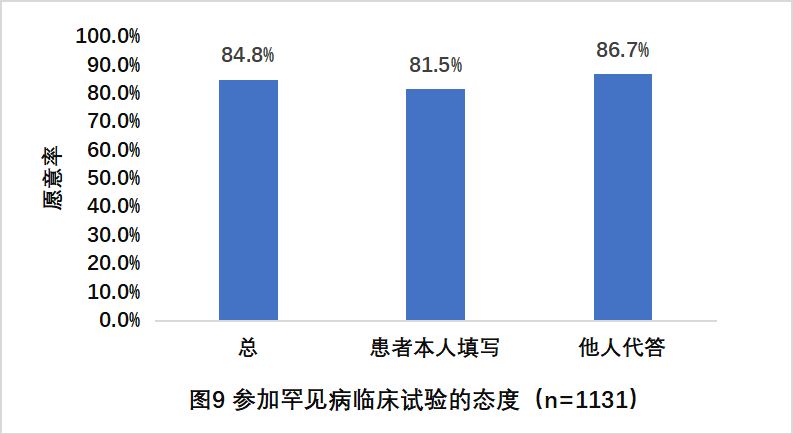
是否愿意参加罕见病临床试验的总态度(图9)
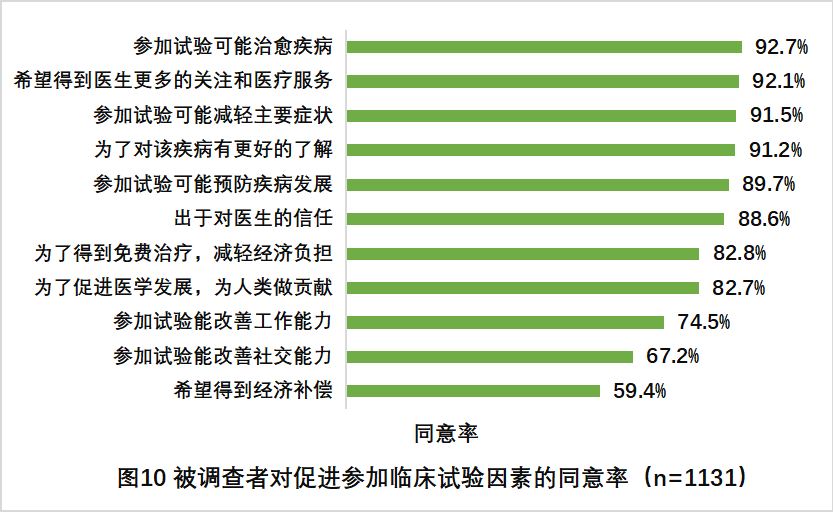
被调查者对促进参与临床试验因素的态度(图10)
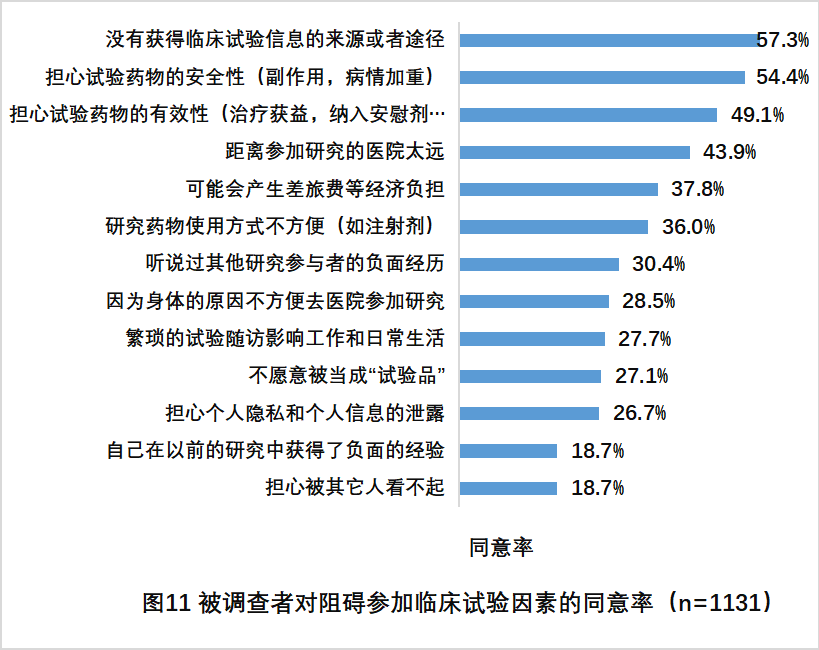
被调查者对阻碍参与临床试验因素的态度(图11)
五.调查结论
1.七成以上(75.5%)的被调查罕见病患者/家属听说过临床试验。其中,女性、低学历、无任何医保者、农村户口的被调查人群对临床试验的知晓率较低。
2.多数被调查者对临床试验基本常识有一定了解,但对个别问题知晓率偏低。比如33.9%的被调查者不知道“患者也可以参与设计和发起符合自己需要的临床试验”。开展临床试验的相关科普工作时,应加强对相关常识和权益的深入普及。
4.关于临床试验信息来源,62.0%的被调查者选择了网络社交软件(比如微信、QQ、论坛、朋友圈等)或新媒体(公众号、微博等),50%选择了罕见病组织。
5.被调查者对于自己或患者参加罕见病临床试验的意愿率分别达到了84.8%,但是实际参加过临床试验的被调查患者占比仅8.9%。而显示临床试验参与渠道不通畅,被调查者参与临床试验的高意愿率和实际的低参与率形成了很大落差。
6.被调查者参与罕见病临床试验的促进因素前三名分别是“参加试验可能治愈疾病”,“希望得到医生更多的关注和医疗服务”,“参加试验可能减轻主要症状”。显示患者/家属对于参加临床试验的好处的主要关注点还是在于对疾病的治疗和医疗服务,也反映了罕见病患者的药物可及性及临床需求还远远没有得到满足。
7.被调查者参与罕见病临床试验的阻碍因素前三名分别为“没有获得临床试验信息的来源或者途径”,“担心试验药物的安全性(副作用,病情加重)”,“担心试验药物的有效性(治疗获益,纳入安慰剂组)”。显示患者/家属对于参加临床试验的障碍的主要关注点在于缺乏信息来源以及对临床试验的安全性和有效性的担忧。
六.对策建议
1.加强罕见病患者/家属的临床试验科普,提高临床试验素养。
2.建立罕见病临床试验信息发布平台,促进临床试验信息共享。
3. 充分发挥患者组织在促进罕见病药物临床试验中的作用。
4. 罕见病临床试验要实现以患者为中心,真正满足罕见病患者未满足的临床需求、心理需求和社会需求。
调查问卷的最后一个问题是开放性提问:“关于罕见病临床试验,您还有什么期待与建议?”,共有1033名被调查者对此问题做了回复。其中,539人表达了对治疗药物上市和纳入医保的迫切愿望。399人表达了希望自己或自己所代表的患者参加临床试验的迫切愿望。256人表达了希望获得临床试验相关信息的愿望或者缺乏临床试验信息来源及参与渠道的困难。另外,很多被调查者表达了对临床试验安全性、参与方便性、经济负担、信息透明、参加机会少,隐私保护、希望有机会参与国外多中心试验等的关注。
以下是部分患者留言。让我们一起倾听一下罕见病患者的心声吧!
本研究研究团队成员如下:
郑航(重庆医科大学药学院药品政策与评价研究中心)
黄如方(蔻德罕见病中心)
向子玲(重庆医科大学药学院药品政策与评价研究中心)
谢生荣(上海柯西医药科技发展有限公司)
李林国(蔻德罕见病中心)
贾芊芊(蔻德罕见病中心)
彭菲菲(重庆医科大学药学院药品政策与评价研究中心)
特向为本调查研究的问卷设计、问卷收集和问卷分析做出重要贡献的同仁致谢:马茗舒、史成桥、王英、王立新等。
还要向为本调查研究的问卷收集做出重要贡献的以下患者组织致谢:
罕见病网络成员组织
你并不孤单FSHD患者关爱组织
朗格罕天使之家
北京企鹅之家小脑萎缩症病患关爱中心
皮宝宝关爱中心
骨力关爱中心
为爱深呼吸IPF关爱中心
淀粉人TTR之家
中国黏多糖I型患者联盟
紫贝壳公益
小胖威利罕见病关爱中心
同时,我们也向每一位填写此报告调研问卷的患者或患者家属致以最诚挚的敬意!
点击链接下载报告:
http://www.raredisease.cn/source!downSource?id=8a9d475474d4bb32017fd4dd5227060d